R2SP : un complexe dynamique au cœur de l’assemblage des cils mobiles
Un article récemment publié par des scientifiques dans Nature Communications lève le voile sur le fonctionnement d’un complexe protéique humain indispensable à la formation de cils mobiles. Grâce à des techniques de pointe en biologie structurale, ils décrivent les mécanismes moléculaires qui sous-tendent son fonctionnement, permettant de mieux comprendre certaines maladies rares, les ciliopathies, qui se manifestent par des troubles respiratoires chez les enfants et/ou une infertilité masculine.
Un acteur central mais encore mystérieux
Les cils mobiles sont de minuscules structures présentes à la surface de certaines cellules. Ils jouent un rôle crucial dans des fonctions vitales : évacuation du mucus dans les voies respiratoires ou propulsion des spermatozoïdes, par exemple. Leur bon fonctionnement dépend d’un assemblage extrêmement précis de protéines.
Parmi les acteurs clés de ce processus figure le complexe multiprotéique R2SP, un chaperon moléculaire chargé d’aider d’autres protéines à adopter la bonne structure tridimensionnelle. Lorsque ce système est défaillant, notamment en cas de mutations dans l’une des protéines du complexe, la protéine SPAG1, cela peut entraîner des ciliopathies, comme la dyskinésie ciliaire primitive, caractérisée par des infections respiratoires chroniques infantiles ou une infertilité masculine.
Malgré son importance, le fonctionnement précis de R2SP restait jusqu’ici mal compris.
Une exploration structurale à haute résolution
Pour percer ce mystère, les scientifiques ont combiné plusieurs techniques complémentaires de biophysique et de biologie structurale :
- la cryo-microscopie électronique (cryo-EM), qui va donner une vue 3D du système global, proche de l’échelle atomique.
- la spectrométrie de masse structurale, qui va affiner les zones de contact du modèle.
- la résonance magnétique nucléaire (RMN), qui révèle la structure 3D de certaines sous-parties, les mouvements et ajustements fins du modèle.
- et la résonance plasmonique de surface (SPR), qui montre la coopérativité de certaines protéines.
Cette approche intégrée a permis de reconstruire l’architecture du complexe avec une résolution remarquable de 3,6 Ångströms, offrant une vision quasi atomique de son organisation.
Une machine moléculaire flexible et coopérative
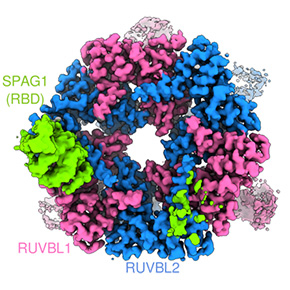
L’étude révèle que le R2SP s’organise autour d’un anneau formé de six ATPases : trois RUVBL1 et trois RUVBL2. Sur cette structure viennent se fixer deux protéines adaptatrices, SPAG1 et PIH1D2.
Contrairement à des complexes similaires, ces deux adaptateurs ne fonctionnent pas indépendamment. Ils interagissent de manière coopérative, ce qui :
- renforce fortement leur fixation sur l’anneau (affinité nanomolaire),
- stimule l’activité enzymatique du complexe,
- et favorise la libération d’ADP, une étape clé du cycle énergétique.
Autre découverte majeure : jusqu’à trois paires SPAG1–PIH1D2 peuvent se fixer simultanément sur un même anneau, conférant au complexe une grande flexibilité structurelle.
Une adaptabilité essentielle pour assembler les moteurs des cils
Cette flexibilité suggère que le R2SP agit comme une pieuvre, capable de recruter différents « clients » protéiques avec ses bras. Parmi eux figurent les dynéines axonémales, des moteurs moléculaires indispensables au mouvement des cils.
En facilitant leur assemblage correct, le R2SP joue donc un rôle central dans la mise en place et le fonctionnement de cils fonctionnels.
Vers une meilleure compréhension des ciliopathies
Ces résultats apportent un éclairage nouveau sur les mécanismes moléculaires à l’origine de certaines maladies rares. En comprenant mieux comment le R2SP fonctionne et dysfonctionne, les scientifiques ouvrent la voie à de futures stratégies thérapeutiques ciblées.
Cette étude illustre aussi la puissance des approches structurales modernes pour décrypter les machines moléculaires complexes au cœur du vivant.

Figure : Structure tridimensionnelle du complexe R2SP révélée par cryo-EM. Cette image montre un modèle global issu de l’intégration des données de cryo-microscopie électronique, RMN et spectrométrie de masse structurale en vue latérale. L'anneau central est formé par trois ATPases RUVBL1 (en rose) et trois ATPases RUVBL2 (en bleu), tandis que les protéines adaptatrices SPAG1 (en vert clair et foncé) et PIH1D2 (rouge/orange) se fixent de manière coopérative sur cet anneau. La flexibilité de cette structure permet à R2SP de s’adapter à différents clients protéiques, jouant ainsi un rôle clé dans l’assemblage des cils mobiles.
En savoir plus : Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Contact
Laboratoires
Laboratoire d’Ingénierie Moléculaire, Cellulaire et Physiopathologie - IMoPA (CNRS/Université de Lorraine)
9 avenue de la forêt de Haye
54505 Vandoeuvre-Lès-Nancy
Institut Plurisciplinaire Hubert Curien – IPHC (CNRS/Université de Strasbourg)
Laboratoire de Spectrométrie de Masse BioOrganique
25 Rue Becquerel
67087 Strasbourg Cedex
Laboratoire de Biologie Moléculaire, Cellulaire et du Développement MCD (CNRS/ Université de Toulouse)
Centre de Biologie Intégrative
169 rue Marianne Grunberg Manago
31062 Toulouse
Infrastructures et plateformes
- Infrastructure Nationale de Protéomique (ProFI) – Site Strasbourg
- Infrastructure Nationale spécialisée dans le domaine de l’imagerie biologique et des technologies de microscopie pour la compréhension du vivant – France-BioImaging (FBI)
- Plateforme de Microscopie Electronique Intégrative (METI) – TRI IBISA FBI- GenoToul
- Centre de Biologie Intégrative (CBI) Toulouse