Glioblastome : quand une molécule suspend le mouvement des cellules tumorales
Les glioblastomes, tumeurs cérébrales particulièrement agressives, résistent aux traitements en grande partie à cause de la présence d’une catégorie de cellules appelées cellules souches tumorales. Dans un article publié dans Cell Reports, des scientifiques révèlent que la protéine JAMC freine l’invasion des cellules souches de glioblastome (GSCs) dans le cerveau. Elle agit comme un frein naturel à leur propagation en limitant leur adhérence aux vaisseaux sanguins.
Glioblastomes et cellules souches tumorales
Les glioblastomes sont les tumeurs du cerveau parmi les plus agressives chez l’adulte. Les échecs des thérapies s’expliquent en partie par la présence de cellules souches tumorales (GSCs). Ces cellules sont capables d’initier la formation des glioblastomes, de se déplacer dans le cerveau et de relancer la croissance tumorale après les traitements.
Dans un article publié dans la revue Cell Reports, des scientifiques ont identifié un régulateur clé de l’interaction entre ces cellules tumorales et les vaisseaux sanguins du cerveau. L’équipe montre que la molécule d’adhérence JAMC (Junctional Adhesion Molecule C) joue un rôle central dans la distribution des GSCs : elle fige les cellules à la paroi externe des vaisseaux et freine ainsi leur dissémination. Ce mécanisme agit via le contrôle d’autres protéines appelées intégrines, essentielles à l’ancrage des cellules dans leur environnement.
Les cellules souches de glioblastome exploitent en effet les vaisseaux sanguins du cerveau pour deux raisons : rester dans des zones dites niches protectrices où elles se multiplient (GROW), et migrer dans le tissu cérébral à distance (GO). Ce phénomène appelé "co-option vasculaire" reste mal compris, notamment en ce qui concerne les molécules d’adhérence impliquées.
JAMC, un frein naturel contre la propagation tumorale
Pour mieux comprendre ce mécanisme, les scientifiques ont combiné plusieurs approches expérimentales :
- Cultures de cellules de patients atteints de glioblastome obtenues lors de biopsies.
- Co-culture de ces cellules avec des cellules endothéliales cérébrales (cellules des vaisseaux sanguins) ou avec des matrices extracellulaires naturellement produites par ces cellules endothéliales.
- Utilisation de tranches de cerveau de souris permettant de conserver la structure tissulaire.
Les résultats montrent que l’absence d’expression et d’activité de JAMC provoque une modification de la morphologie des GSCs et une migration accrue le long des vaisseaux. Cela conduit à une invasion tumorale accélérée dans le cerveau et une réduction significative de la survie de souris greffées avec ces cellules.
Ces observations ont été confirmées par une analyse de tissus humains : l’analyse de l’expression des gènes montre que les zones tumorales les plus invasives présentent une faible expression de JAMC. Parallèlement, une analyse de l’ensemble des protéines a révélé un lien inédit entre l’activité de JAMC et celle des intégrines, via une protéine appelée SHARPIN, connue pour limiter l’activité des intégrines. Ce réseau de signalisation apparaît crucial pour moduler l’adhérence et le comportement migratoire des cellules souches tumorales.
En révélant le rôle de JAMC comme "frein" naturel de l’invasion des GSCs, cette étude ouvre de nouvelles perspectives pour mieux comprendre les mécanismes de propagation du glioblastome, et identifier des cibles thérapeutiques capables de limiter la dissémination de ces cellules résistantes.
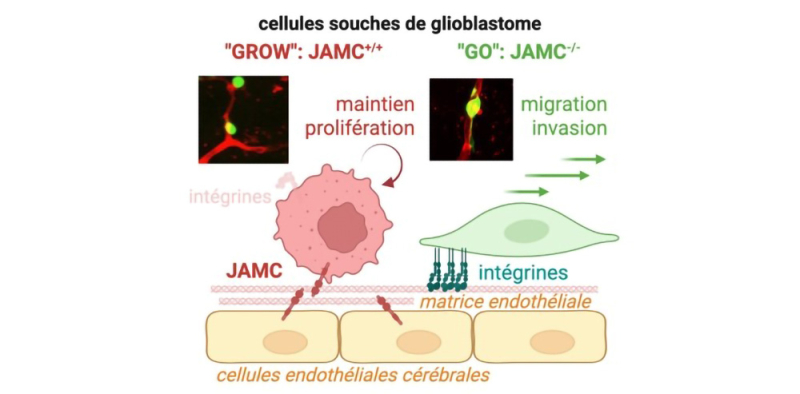
Figure : Les cellules souches de glioblastome (GSCs) interagissent étroitement avec les cellules endothéliales cérébrales, adoptant deux comportements complémentaires : un état prolifératif et de maintien de leurs propriétés souches ("GROW", à gauche) lorsqu’elles expriment JAMC, et un état migratoire invasif ("GO", à droite) en l’absence de cette molécule d’adhérence. Lorsque JAMC est exprimée à la surface des GSCs, l’activité des intégrines est régulée négativement, limitant ainsi leur adhérence à la surface endothéliale et leur capacité à migrer. À l’inverse, l’absence de JAMC favorise l’invasion tumorale en renforçant l’ancrage des GSCs à l’environnement vasculaire, via les intégrines. Ces résultats soulignent le rôle central de JAMC comme frein naturel de la dissémination tumorale dans le cerveau.
En savoir plus : Sara Rosińska, Gwennan André-Grégoire, Mathilde Kerhervé et al. Junctional adhesion molecule C limits glioblastoma stem-like cell invasion by regulating integrin adhesion at the endothelial interface Cell Rep (2025) https://doi.org/10.1016/j.celrep.2025.116194
Contact
Laboratoire
Centre de recherche en cancérologie et immunologie intégrée Nantes-Angers - CRCI2NA (CNRS/Inserm/Nantes Université/Université d'Angers)
8 quai Moncousu
44007 NANTES CEDEX 1 - France


