Cancer du cerveau : comment le cholestérol inonde les cellules souches du glioblastome
Les cellules souches du glioblastome représentent un réservoir de cellules contribuant à la formation et à la résistance de ces tumeurs du cerveau. Dans un article publié dans la revue Cell Reports les scientifiques montrent que la viabilité de ces cellules prélevées sur les tumeurs des patients dépend de la quantité disponible en cholestérol cellulaire.
Le glioblastome est le plus commun et le plus meurtrier des cancers du système nerveux central de l’adulte. Malgré un protocole standard de prise en charge établi en 2005, combinant une chirurgie maximale suivie de séances de radio- et chimiothérapies, les patients survivent en moyenne seulement 15 mois après leur diagnostic. Cette agressivité est notamment liée à la présence de cellules souches cancéreuses appelées cellules de type souche du glioblastome, ou GSCs. Ces cellules, impliquées dans l’initiation, la croissance, et la rechute de la tumeur, représentent donc des cibles préférentielles pour l’élaboration de nouvelles stratégies thérapeutiques.
Les lysosomes jouent un rôle critique dans le maintien des cellules souches cancéreuses
Les lysosomes, éléments constitutifs de la cellule, forment un réseau dynamique de vésicules (sorte de petits sacs), au pH acide, impliquées dans le déplacement des substances à l'intérieur de la cellule. Ils participent aux processus métaboliques, et sont responsables de la digestion des particules ingérées par la cellule et de la dégradation des composants cellulaires défectueux.
Des travaux antérieurs montrent qu’ils permettent, en outre, la survie des cellules souches du glioblastome hors de leur niche protectrice au sein de la tumeur. En effet, les lysosomes prolongent les signaux des facteurs de croissance et facilitent la diffusion et la prolifération des cellules cancéreuses. Dans les cellules souches du glioblastome, le fait d’altérer la quantité et la qualité des lysosomes entraine une mort spécifique de ces cellules. Les lysosomes sont ainsi une cible thérapeutique critique pour influer les décisions vie-et-mort de ces cellules souches du glioblastome et ainsi contrôler leur population.
Pour déstabiliser la paroi des petits sacs que sont les lysosomes, au cœur des cellules souches du glioblastome, les scientifiques ont identifié le rôle de la protéase MALT1 (de la famille des paracaspases). Le fait d’inhiber cette enzyme, récemment définie comme un médiateur crucial de l’homéostasie des lysosomes, aboutit en une mort lysosome-dépendante des cellules souches du glioblastome. Ce, via un mécanisme impliquant la protéine de liaison à l’ARNm Quaking et la modulation de l’expression des protéines clés du compartiment lysosomal. Cependant, les mécanismes d’action de MALT1 restent encore mal caractérisés.
Un déluge de cholestérol lysosomal pour détruire les cellules souches du glioblastome
Aujourd’hui, les résultats de cette étude permettent de mieux comprendre les rouages du système. En effet, ils suggèrent que la répression de MALT1, par des agents pharmacologiques ou par interférence à l’ARN (technique qui permet d’inhiber spécifiquement la synthèse de la protéine en détruisant le messager qui lui correspond), modifie l'homéostasie (l’équilibre entre l’intérieur et l’extérieur) du cholestérol. Le cholestérol s'accumule alors dans les vésicules du compartiment des lysosomes et des endosomes tardifs. Cette défaillance de l'approvisionnement en cholestérol aboutit à la mort cellulaire et à des défauts d'autophagie (système d’auto-nettoyage de la cellule), qui peuvent être partiellement inversés en fournissant aux cellules souches du glioblastome, du cholestérol perméable à la membrane. Ces résultats ont pu être obtenus grâce à la combinaison d'une analyse par séquençage de l'ARN (RNA-seq) et d'une quantification du protéome, réalisée sur des cellules souches du glioblastome dérivées de patients et soumises à un inhibiteur pharmacologique de l'activité protéolytique de MALT1.
D'un point de vue moléculaire, une analyse ciblée du protéome des lysosomes a révélé que les transporteurs de cholestérol lysosomal de type Niemann-Pick C (NPC) sont moins présents lorsque l’activité de MALT1 est entravée. En accord avec ces données, bloquer pharmacologiquement ou éteindre l’expression de ces transporteurs NPC1/2 reproduit les effets de la perte-de-fonction de MALT1, suggérant une action similaire de ces deux molécules. Enfin, l’inhibition de MALT1 ou de NPC1/2 ralentit la croissance tumorale dans des modèles de souris immunodéprimées, portant des cellules souches du glioblastome provenant de patients.
Ce travail a donc permis la cartographie des événements au niveau subcellulaire, participant à la déstabilisation lysosomale induite par le ciblage moléculaire et pharmacologique de la paracaspase MALT1. Ces données font émerger l’idée selon laquelle les propriétés et le maintien des cellules souches du glioblastome reposent sur l’homéostasie du cholestérol lysosomal.
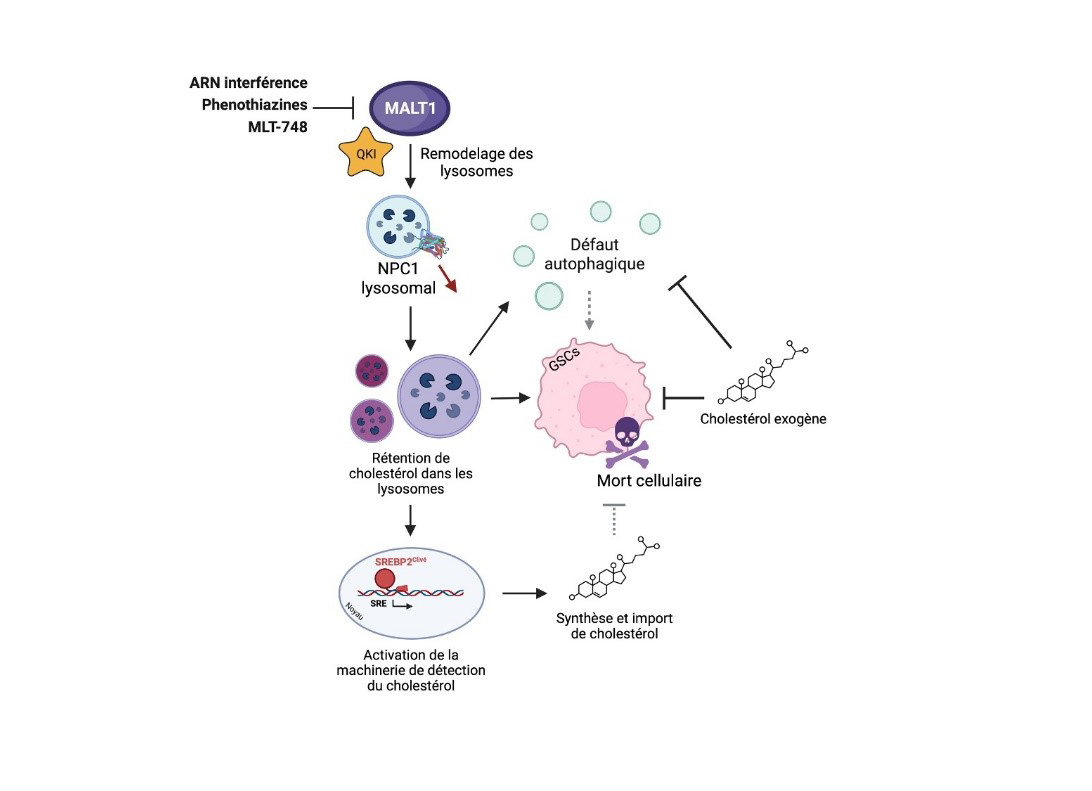
Figure : Modèle d’action de MALT1 dans le maintien de l’homéostasie lysosomale
La protéase MALT1 module la localisation lysosomale de la protéine NPC1 et l'homéostasie du cholestérol. Dans les cellules de type souche du glioblastome (GSCs), inhiber l'activité de la paracaspase MALT1 ou interférer avec son niveau d’expression remodèle le compartiment lysosomal, en réduisant notamment la quantité du transporteur de cholestérol NPC1. S'en suit une rétention intra-lysosomale de cholestérol, induisant un défaut de la dégradation autophagique, l'activation de la machinerie permettant l'import et la synthèse de cholestérol, et finalement, la mort cellulaire des GSCs. Ajouter du cholestérol exogène sur des GSCs dont l'activité de MALT1 a été inhibée permet de partiellement contrecarrer les phénotypes mentionnés précédemment, plaçant ainsi le transport lysosomal du cholestérol comme une cible des GSCs.
En savoir plus :
The paracaspase MALT1 controls cholesterol homeostasis in glioblastoma stem-like cells through lysosome proteome shaping. Maghe C, Trillet K, André-Grégoire G, Kerhervé M, Merlet L, Jacobs KA, Schauer K, Bidère N, Gavard J. Cell Rep. 2024 Jan 5;43(1):113631. doi: 10.1016/j.celrep.2023.113631.
Contact
Laboratoire
Centre de recherche en cancérologie et immunologie intégrée Nantes-Angers - CRCI2NA (CNRS/Inserm/Nantes Université/Université d'Angers)
8 quai Moncousu
44007 NANTES CEDEX 1 - France