Division bactérienne : Un signal transitoire positionne le site de division chez les streptocoques
Streptococcus pneumoniae présente des spécificités dans son mode de division. Dans un article publié dans Nature Microbiology, des scientifiques décryptent le mécanisme moléculaire qui permet d’assurer, chez cette espèce, une division en deux cellules filles identiques. Ces recherches fondamentales ouvrent des pistes pour cibler des molécules capables de perturber la division de cette bactérie pathogène.
La plupart des bactéries se multiplient par fission binaire, un processus simple en apparence : une cellule mère se divise en deux cellules filles identiques. Mais cette opération exige une précision remarquable.
Au cœur du mécanisme se trouve le divisome, un complexe multiprotéique chargé de scinder la cellule mère et de construire une nouvelle paroi entre les deux futures cellules. Cette paroi est composée de peptidoglycane, un maillage solide de sucres reliés par de courts peptides.
Dans de nombreuses bactéries, des systèmes dits négatifs empêchent le divisome de s’assembler ailleurs qu’au centre de la cellule mère. Mais certaines, comme les streptocoques, ne possèdent pas ces garde-fous et utilisent à la place une stratégie différente : un système positif qui marque activement le futur site de division et positionne le divisome.
MapZ : au cœur du système positif de marquage du futur site de division
Ce système positif repose sur une protéine membranaire appelée MapZ, véritable guide qui indique où assembler le divisome. Des travaux antérieurs avaient montré que MapZ reconnaît une signature spécifique dans le peptidoglycane, sans que la nature de ce signal soit clairement identifiée. Dans un article publié dans la revue Nature Microbiology, les scientifiques ont réussi à identifier cette signature chez Streptococcus pneumoniae. Elle repose sur des modifications très précises des peptides qui relient les chaînes de sucres du peptidoglycane.
Deux enzymes jouent un rôle clé :
- DacA, qui enlève le 5ᵉ acide aminé du peptide,
- DacB, qui retire ensuite le 4ᵉ acide aminé.
Ce processus crée donc, pendant un court laps de temps, une forme intermédiaire, un tétrapeptide généré par DacA avant qu’il ne devienne un tripeptide suite à l’action de DacB.
Une fenêtre temporelle décisive
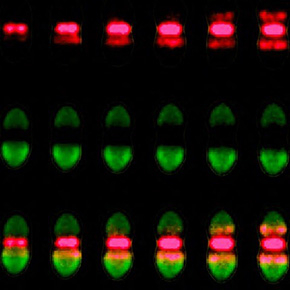
Les résultats des expériences montrent que la localisation de MapZ est fortement compromise dans des mutants déficients pour l’expression de dacA ou dacB. Plus précisément, MapZ ne peut plus se positionner au futur site de division en l’absence de DacA alors qu’elle est capable de se positionner de manière anarchique et instable en l’absence de DacB. Pour confirmer ces résultats, les scientifiques ont suivi la localisation de DacA et de DacB au cours du cycle cellulaire. Les expériences montrent un léger décalage du timing de localisation de ces deux protéines. DacA localise en premier au site de division et est rapidement suivi par DacB. Ceci indique que pendant une courte fenêtre de temps, la paroi cellulaire au niveau du site de division contient un tétrapeptide, résultant de l’action de DacA mais n’ayant pas encore été hydrolysé et transformé en tripeptide par DacB. Cette fenêtre coïncide avec la localisation de MapZ au site de division, qui interagit alors avec cette signature.
Un nouveau modèle de division
Ces résultats conduisent à un modèle inédit : la position du site de division n’est pas définie par une structure permanente, mais par un signal transitoire inscrit dans la paroi cellulaire elle-même.
MapZ agit alors comme un capteur de cette signature, permettant son ancrage à un site qui deviendra le site de division.
À terme, ces données pourraient servir de base fondamentale à des travaux plus appliqués pour développer des molécules affectant la reconnaissance de la signature par MapZ et ainsi induire des défauts de division impactant la division et la multiplication des Streptocoques et par conséquent limitant leur pouvoir infectieux.
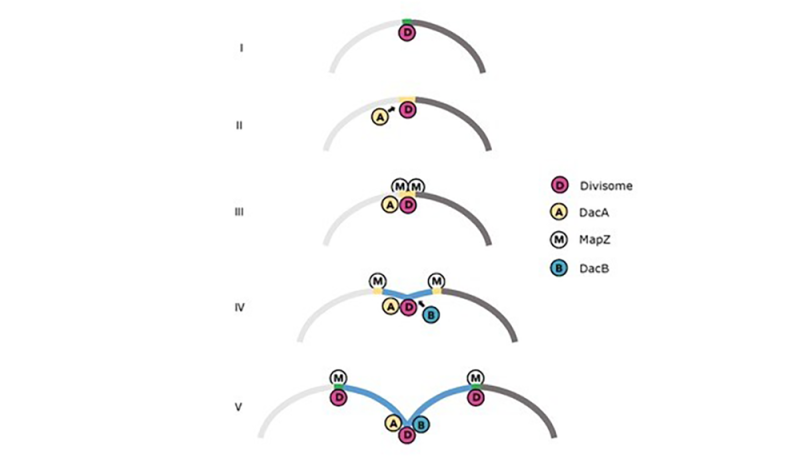
Figure : Modèle illustrant le positionnement de la protéine MapZ (M) au centre de la cellule de Streptococcus pneumoniae. Lorsque la division commence (I), le divisome (D) se localise au centre de la cellule et produit du peptidoglycane (vert). En présence de DacA (A) et en l'absence de DacB (B), la plupart des peptides sont coupés par DacA (jaune) (II) et sont spécifiquement reconnus par MapZ (III). À mesure que le peptidoglycane continue d’être synthétisé, il est progressivement repoussé vers l'extérieur du site de division, le rendant inaccessible à DacB (B) (IV). En présence de DacB, la plupart des peptides sont coupés (bleu) et ne sont plus reconnus par MapZ (IV à V). Lorsque la formation du septum est achevée (V), le divisome se repositionne vers les anneaux MapZ situés à l'équateur des cellules filles pour amorcer un nouveau cycle.
En savoir plus : Ducret, A., Falcou, C., Freton, C. et al. Local peptidoglycan composition defines division site selection in Streptococcus pneumoniae. Nat Microbiol (2026). https://doi.org/10.1038/s41564-026-02322-6
Contact
Laboratoire
Laboratoire microbiologie moléculaire et biochimie structurale - MMSB (CNRS/Université Lyon 1)
7, passage du Vercors
69367 Lyon
France