Assembler la paroi bactérienne : une mécanique finement orchestrée
La forme cellulaire des bactéries repose sur l’assemblage d’un polymère extracellulaire appelé peptidoglycane. La synthèse de ce polymère qui protège également la cellule bactérienne des stress physiques et chimiques de son environnement est par conséquent finement contrôlé. Dans un article publié dans Nature Microbiology, des scientifiques ont identifié un complexe protéique essentiel pour le remodelage du peptidoglycane et la protection de la cellule bactérienne en cours de division.
Le peptidoglycane : un matériau vital et une cible thérapeutique majeure
Le peptidoglycane est le composant majeur de la paroi cellulaire des bactéries. Cette structure rigide forme une véritable cage protectrice qui confère à la cellule bactérienne sa forme et lui permet de résister aux contraintes de son environnement. La synthèse de ce polymère est donc vitale et finement régulée, notamment lors de la division cellulaire, lorsque de nouveaux fragments doivent être insérés avec précision dans une paroi préexistante.
Cette étape cruciale est la cible de nombreux antibiotiques utilisés en clinique pour lutter contre les infections bactériennes. Ces antibiotiques ciblent notamment les PBP (Penicillin-Binding-Protein), des enzymes responsables de la polymérisation du peptidoglycane. Si les PBPs impliquées sont bien caractérisées, les mécanismes moléculaires coordonnant leurs activités restent encore largement méconnus, notamment pour assurer la coordination de leur activité avec celles d’autres enzymes afin d’obtenir un peptidoglycane mature.
La protéine S, un acteur central de la morphogénèse bactérienne
Pour résoudre cette inconnue, des scientifiques, dans un article publié dans la revue Nature Microbiology, ont utilisé une approche pluridisciplinaire associant génétique bactérienne, biochimie, phylogénomique, microscopie et intelligence artificielle. Cette approche pluridisciplinaire leur a permis d’identifier la protéine membranaire S, codée par le gène ess, comme un acteur indispensable de la synthèse du peptidoglycane et la morphogénèse de la bactérie Streptococcus pneumoniae.
Ils montrent que la protéine S se localise précisément au site de division cellulaire. La suppression du gène ess provoque une altération sévère de la forme de bactérie, soulignant son rôle essentiel dans le maintien de l’intégrité cellulaire.
L’étude révèle que le domaine extracellulaire de la protéine S présente une région flexible lui permettant d’interagir spécifiquement avec PBP1a. Cette interaction est déterminante pour activer PBP1a et déclencher la polymérisation des chaînes glucidiques du peptidoglycane, étape clé de la construction de la paroi.
Un réseau d’interaction pour remodeler la paroi
Les scientifiques mettent également en évidence une coopération étroite entre deux systèmes enzymatiques. Le gène ess devient indispensable lorsqu’une seconde PBP, la PBP2a, ou son activateur MacP, n’est plus produite. Cette observation indique que les paires MacP/PBP2a et ProteinS/PBP1a agissent de concert pour remodeler le peptidoglycane.
Le domaine cytoplasmique de la protéine S possède un motif d’interaction spécifique avec une protéine clé de la division cellulaire GpsB, impliquée dans le contrôle de l’allongement et la constriction cellulaire. Ce motif d’interaction est également retrouvé dans la protéine PBP2a et chez les protéines MpgA et PdgA qui clive et modifie par désacétylation le peptidoglycane, respectivement. L’ensemble des gènes codant ces protéines présente en outre de nombreuses interactions génétiques négatives ou positives renforçant l’idée d’un lien fonctionnel étroit.
Vers une vision intégrée de l’assemblage du peptidoglycane
En réunissant ces résultats, les scientifiques proposent l’existence d’un complexe moléculaire coordonné par la protéine GpsB dans lequel agissent de manière synchronisée deux PBP et leurs régulateurs respectifs, d’une hydrolase facilitant l’insertion du nouveau peptidoglycane produit et d’une enzyme de modification du peptidoglycane susceptible de modifier l’activité de l’ensemble du complexe.
Cette découverte apporte un éclairage nouveau sur les mécanismes d’assemblage du peptidoglycane. Au-delà de l’intérêt fondamental, ces travaux ouvrent la voie à de nouvelles stratégies thérapeutiques, pour interférer sur la synthèse du peptidoglycane et ainsi fragiliser la cellule bactérienne pour limiter sa dissémination lors d’une infection bactérienne.
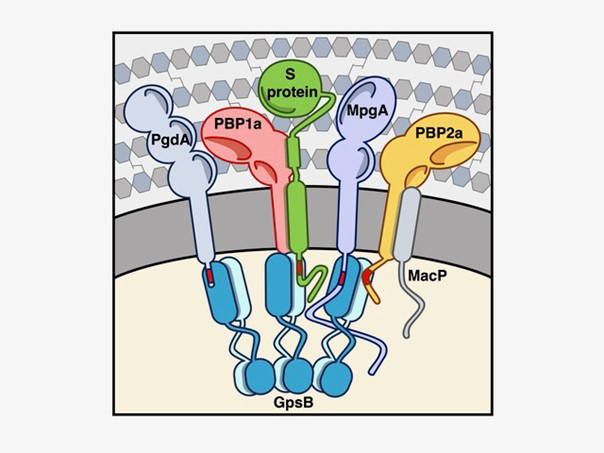
Figure : Modèle du complexe protéique dans lequel le dialogue moléculaire entre GpsB et PBP1a et PBP2a, leur régulateurs respectifs, la protéine S et MacP, la désacétylase PgdA et l’hydrolase MpgA contrôle le remodelage du peptidoglycane au cours du cycle cellulaire du pneumocoque.
En savoir plus : Millat, H., Falcou, C., Lenoir, C. et al. Streptococcus pneumoniae S protein activates PBP1a to regulate peptidoglycan remodelling and cell division. Nat Microbiol (2025). https://doi.org/10.1038/s41564-025-02210-5
Contact
Laboratoire
Microbiologie moléculaire et biochimie structurale - MMSB (CNRS/Université Claude Bernard)
7, passage du Vercors
69367 Lyon
France