Une preuve de concept préclinique de thérapie génique pour le syndrome de l’X fragile
Le syndrome de l’X fragile (FXS) représente la première cause de déficience intellectuelle familiale pour lequel aucun traitement n’existe actuellement. Dans cette étude publiée dans la revue EMBO Molecular Medicine, les scientifiques étudient le rôle de l’enzyme DGKk, déficiente dans cette pathologie. Ils observent que la réexpression de cette enzyme chez des souris jeunes adultes corrige à long terme leurs perturbations moléculaires et leurs principaux troubles comportementaux. Ces résultats soutiennent un rôle important du dysfonctionnement de l’enzyme DGKk dans cette pathologie.
Le syndrome de l’X fragile affecte environ un homme sur 4000 et une femme sur 8000. Ce syndrome est dû à une mutation dans le gène FMR1, situé sur le chromosome X, qui provoque la perte d’expression de la protéine FMRP. Cette dernière est une protéine de liaison aux ARN dont l’absence provoque une dérégulation de l’expression de nombreux gènes intervenant dans la communication entre les neurones de plusieurs régions du cerveau.
Des travaux précédents avaient identifié que la protéine FMRP contrôle dans les neurones la fabrication d’une enzyme particulière appelée Diacylglycerol kinase kappa (DGKk). Cette enzyme pourrait représenter une clé du mécanisme pathologique car elle est essentielle à la fabrication de lipides membranaires impliqués dans la signalisation intracellulaire et contrôlant la synthèse des nouvelles protéines nécessaires à la communication neuronale.
Les scientifiques ont testé le postulat selon lequel, si l’enzyme DGKk joue un rôle important dans la pathologie, sa réexpression dans les neurones « X fragile » pourrait avoir la capacité à corriger leurs altérations. Après avoir identifié une forme modifiée de l’enzyme qui n’a plus besoin de la protéine FMRP pour être produite dans les neurones, ils ont apporté l’enzyme DGKk dans les neurones cérébraux des souris modèles de la pathologie au moyen d’un vecteur viral adéno-associé (AAV), utilisé actuellement dans plusieurs essais de thérapie génique chez l’homme. Le traitement réalisé chez des souris jeunes adultes permet d’obtenir une correction des anomalies moléculaires et comportementales avec un effet à long terme (plus de 8 semaines après le traitement).
Ces résultats constituent une indication du rôle important de cette enzyme dans la pathologie et une première preuve de concept préclinique d’un traitement par approche de thérapie génique au stade jeune adulte. Les futurs développements nécessiteront le développement d’un mode d’administration du vecteur applicable à l’homme et des validations dans d’autres modèles.
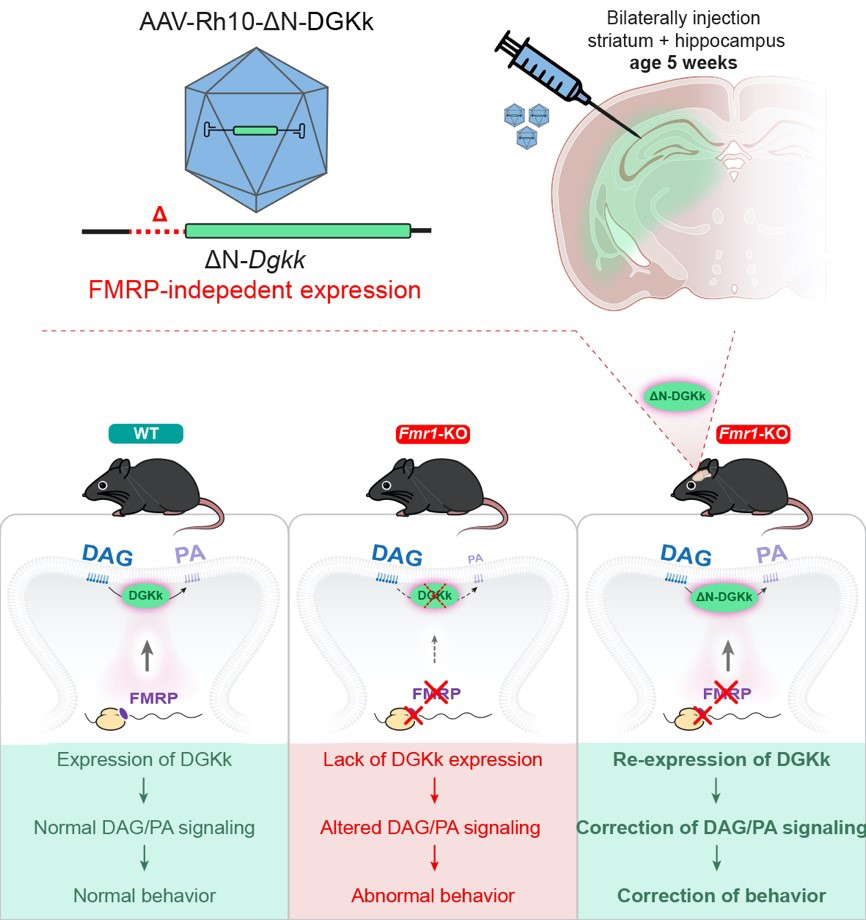
Figure : Le vecteur viral adéno-associé AAV-Rh10-∆N-DGKk, en permettant de réexprimer l’enzyme déficiente DGKk dans les neurones de la souris Fmr1-KO, corrige les déficits moléculaires et comportementaux du modèle préclinique de la maladie du syndrome de l’X fragile. Cette stratégie, plus aisée que d’agir directement sur la protéine FMRP, constitue une première preuve de concept préclinique d’une approche de thérapie génique au stade jeune adulte chez la souris. WT, modèle souris "normal" ; Fmr1-KO, modèle souris "X fragile" ; DAG/PA, signalisation des lipides diacylglycerol et acide phosphatidique.
Pour en savoir plus :
AAV-delivered diacylglycerol kinase DGKk achieves long-term rescue of fragile X syndrome mouse model.
Habbas K, Cakil O, Zámbó B, Tabet R, Riet F, Dembele D, Mandel JL, Hocquemiller M, Laufer R, Piguet F, Moine H.
EMBO Mol Med. 4 avril 2022 doi: 10.15252/emmm.202114649.
Contact
Laboratoire
Institut de génétique et de biologie moléculaire et cellulaire - IGBMC (CNRS/Inserm/Université de Strasbourg)
1 rue Laurent Fries
87404 Ilkirch CEDEX