Une interaction dynamique entre protéine et membrane assure la bonne répartition de l'ADN chez une bactérie pathogène
Lors de la division cellulaire, les bactéries doivent répartir fidèlement leur ADN entre les deux cellules filles. Dans un article publié dans Advanced Science, des scientifiques montrent que, chez la bactérie Streptococcus pneumoniae, cette étape dépend d’une interaction étroite entre la protéine RocS et la membrane cellulaire. Leur étude révèle qu’un court motif conservé de RocS agit comme une ancre membranaire capable d’organiser localement les lipides et de guider la séparation correcte des chromosomes
Une étape cruciale de la division bactérienne
Lorsqu’une bactérie se divise, elle doit transmettre à chacune des deux cellules filles une copie complète de son génome. Cette étape, appelée ségrégation des chromosomes, repose sur des mécanismes moléculaires finement régulés.
Une étude publiée dans Advanced Science apporte un nouvel éclairage sur ce processus chez la bactérie pathogène Streptococcus pneumoniae. Les scientifiques montrent qu’un élément structural très court de la protéine RocS, protéine spécifique de la famille des spectrococcaceae, joue un rôle central dans la répartition correcte des chromosomes lors de la division cellulaire
Cette recherche, menée à l’interface entre chimie et biologie, met en évidence un mécanisme original reposant sur l’interaction directe entre une protéine et la membrane bactérienne.
Une protéine ancrée à la membrane grace à un motif conservé
La protéine RocS est connue pour être essentielle à la ségrégation des chromosomes chez les bactéries du genre Streptococcus. Cependant, son mode d’action restait encore mal compris.
Les scientifiques ont identifié un court motif situé à l’extrémité C-terminale de RocS, fortement conservé entre différentes espèces bactériennes. Ce motif agit comme une ancre membranaire, permettant à la protéine de se fixer directement à la membrane plasmique.
Cette interaction apparaît indispensable pour que RocS puisse remplir correctement sa fonction dans la séparation des chromosomes dupliqués.
Une interaction dynamique entre protéine et membrane bactérienne
Pour comprendre précisément comment ce motif agit, les scientifiques ont combiné plusieurs approches expérimentales : spectroscopie RMN du solide, biophysique des membranes, microscopie à fluorescence et microscopie à force atomique.
Leurs analyses montrent que le motif adopte une structure hélicoïdale précédée d’un “coude” caractéristique lorsqu’il s’insère dans la membrane lipidique. Mais son rôle ne se limite pas à un simple point d’ancrage.
En s’insérant dans la membrane et en permettant le positionnement correct de RocS, ce motif réorganise localement les lipides et cible des nanodomaines membranaires spécifiques. Cette organisation membranaire est essentielle pour assurer la séparation fidèle des chromosomes lors de la division cellulaire.
Un mécanisme potentiellement largement partagé
En reliant des observations allant de l’échelle cellulaire à l’échelle atomique, cette étude révèle comment un simple motif peptidique conservé peut coordonner les interactions entre protéines et membrane pour contrôler un processus biologique majeur.
La présence de motifs similaires chez d’autres bactéries, mais aussi chez certains organismes comme les algues, suggère que ce mécanisme pourrait être largement répandu dans le vivant.
Ces résultats ouvrent ainsi de nouvelles perspectives pour mieux comprendre la communication entre protéines et lipides membranaires et pourraient, à plus long terme, contribuer à l’identification de nouvelles cibles antibactériennes.
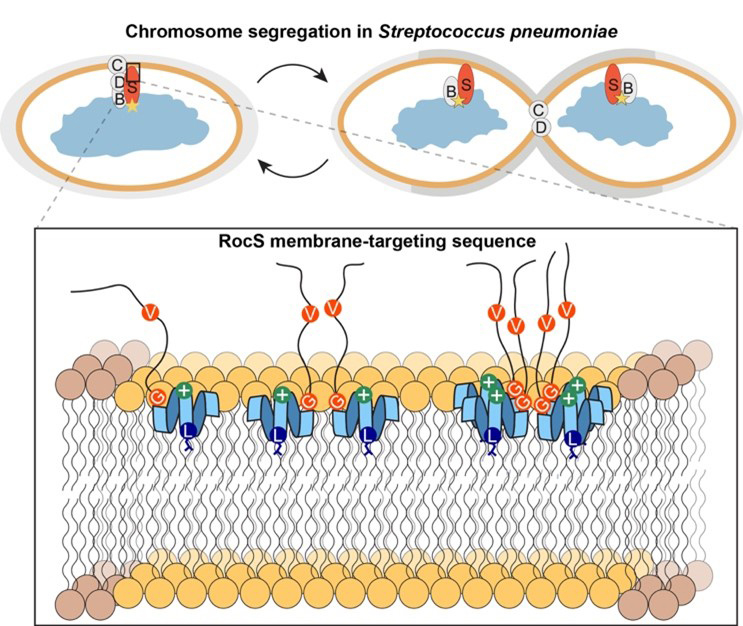
Figure : Modèle mécanistique de l’association de la MTS de RocS avec la membrane. Panneau supérieur : Rôle de RocS (S) de Streptococcus pneumoniae dans la ségrégation des chromosomes. ParB (B) représente le principal partenaire moléculaire au cours de la division cellulaire et l’étoile jaune indique le site de liaison parS de ParB dans la région OriC. Panneau inférieur : Zoom sur la séquence de l’ancre membranaire conservé (membrane targeting sequence MTS). La MTS de RocS s’associe à des nanodomaines membranaires plus fins et s’assemble en foyers oligomériques. L’hélice amphipathique C-terminale (bleu clair) s’insère à la surface de la membrane, précédée par un coude au niveau d’une Glycine conservée (G orange) et une Valine flexible (V orange). La leucine centrale de l’hélice (L bleu) pourrait s’étendre vers la région hydrophobe de la membrane, tandis que le résidu chargé positivement reste à la surface membranaire.
En savoir plus : A.Álvarez-Mena, E.Morvan, C.Lambert, et al. “Structural Basis of the Membrane Association by the Conserved RocS Membrane-Targeting Sequence in Streptococcus.” Advanced Science13, no. 17 (2026): e21132. https://doi.org/10.1002/advs.202521132
Contact
Laboratoires
Laboratoire de Microbiologie Moléculaire et Biochimie Structurale - MMSB (CNRS/Université Lyon 1)
7, passage du Vercors,
69007 Lyon
Institut de Chimie et Biologie des Membranes et des Nano-objets - CBMN (Bordeaux INP/CNRS/Université de Bordeaux)
1 All. Geoffroy Saint-Hilaire,
33600 Pessac