Un rôle pour la protéine SMN, responsable de l’amyotrophie spinale
Les dommages à l’ADN affectent l’organisation du nucléole, structure du noyau des cellules eucaryotes, qui, après réparation, doit retrouver sa structure initiale pour fonctionner efficacement. Dans une étude publiée dans la revue Nature Communications, les scientifiques ont montré que la protéine SMN, en cause dans l’amyotrophie spinale (SMA), est nécessaire pour que le nucléole retrouve son exacte organisation. Par conséquence, le défaut de réorganisation dans les cellules déficientes pour la protéine SMN entraîne une sensibilité aux dommages à l’ADN.
L’amyotrophie spinale et la protéine SMN
L'amyotrophie spinale (SMA) est une maladie neuromusculaire qui affecte les nerfs et les muscles. Elle se caractérise par la dégénérescence des motoneurones de la moelle épinière qui contrôlent les mouvements musculaires. La perte de motoneurones empêche les muscles de recevoir les signaux et engendre une atrophie musculaire progressive et débilitante. Il s'agit de la cause la plus fréquente de maladie mortelle héréditaire chez l'enfant, entraînant généralement la mort au cours de la première année de vie. Les enfants atteints de SMA présentent des difficultés pour ramper, marcher, respirer et avaler. La SMA est causée par des mutations du gène Smn1, qui code pour la protéine Survival of Motor Neuron (SMN). Dans le noyau des cellules, la protéine SMN se localise dans un petit organite appelé les corps de Cajal. Ces corps de Cajal peuvent s’associer à une autre organelle dans le noyau : le nucléole.
Le nucléole et les dommages à l’ADN
Le nucléole est une organelle dans lequel la cellule produit les premières briques de ce qui seront les sites de production des protéines : les ribosomes. Le nucléole a une structure bien précise qui peut être modifiée par le stress cellulaire. En effet, après l’induction de lésions à l’ADN par des agents oxydants ou les ultraviolets, les protéines nucléolaires sont exportées en périphérie du nucléole. Cependant, pour bien fonctionner la cellule doit maintenir une structure correcte du nucléole et donc, après la réparation des dommages à l’ADN, il est nécessaire de restaurer la bonne structure du nucléole.
La protéine SMN maintient l’homéostasie nucléolaire
Dans un article publié récemment dans la revue Nature Communications, les scientifiques ont découvert que la protéine SMN est nécessaire à la restauration de la structure du nucléole et que pour le faire elle se déplace depuis les corps de Cajal vers le nucléole pendant le processus de réparation de l’ADN. Ce déplacement entre les corps de Cajal et le nucléole dépend de la présence d’autres protéines, tel que la coilin (une protéine faisant partie des corps de Cajal), la fibrillarine (une protéine faisant partie du nucléole) et de l’activité enzymatique de la méthyltransférase PRMT1 (Protein Arginine Methyl-Transferase 1). De plus, l’équipe a pu mettre en évidence que les cellules déficientes en SMN sont sensibles aux dommages à l’ADN, notamment les dommages oxydatifs. Ce type de dommages peut perturber les fonctions des cellules, telles que l’expression des gènes et la production de protéines, favoriser le vieillissement cellulaire et ainsi accélérer la dégénération neuronale.
Quel impact pour les patients atteints d’amyotrophie spinale ?
Depuis un certain nombre d’années, il existe des thérapies qui visent à restaurer les niveaux et la fonctionnalité de la protéine SMN. Cependant, ces thérapies sont extrêmement couteuses et ne résolvent pas tous les problèmes liés à la maladie. Il reste donc crucial de continuer à mieux comprendre le processus de la maladie et d'explorer des stratégies alternatives.
La mise en évidence de cette nouvelle fonction de SMN amène les scientifiques à l’hypothèse que dans les cellules et les motoneurones des patients atteints de SMA, le stress cellulaire engendre des perturbations progressives et durables du nucléole, altérant ainsi profondément la formation des ribosomes et entraînant un dérèglement de la production des protéines essentielles à la vie. Les résultats de ces recherches pourraient donc avoir un impact direct sur la vie et le bien-être des patients atteints de SMA, à travers une thérapie concourant à prévenir les dommages à l’ADN et ainsi préserver la structure du nucléole qui affecte la bonne production de protéines dans leurs cellules.
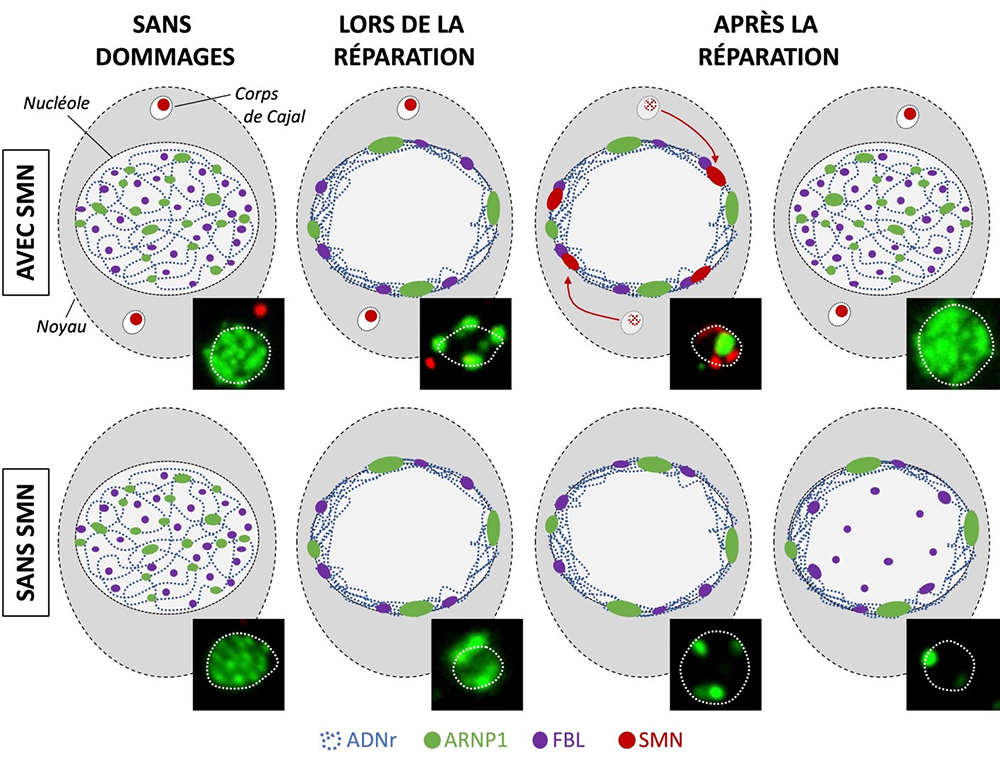
Figure : La réorganisation du nucléole pendant la réparation dépend de la protéine SMN.
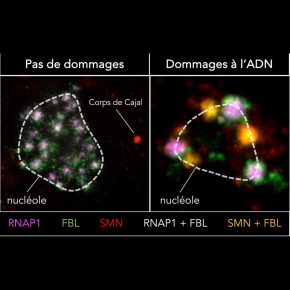
Après un stress génotoxique, l’ARN polymérase 1 (ARNP1 en vert), la Fibrillarine (FBL en violet) et l’ADN nucléolaire (ADNr en bleu) sont exportés vers la périphérie du nucléole. Pendant la réparation de l’ADN, SMN (en rouge) se déplace des corps de Cajal vers le nucléole. Une fois la réparation de l’ADN entièrement terminée, l’organisation du nucléole est restaurée. Cette restauration dépend de la présence de SMN.
En savoir plus :
Musawi, S., Donnio, LM., Zhao, Z. et al. Nucleolar reorganization after cellular stress is orchestrated by SMN shuttling between nuclear compartments. Nat Commun 14, 7384 (2023). https://doi.org/10.1038/s41467-023-42390-4
Contact
Laboratoire
Pathophysiologie et génétique du neurone et du muscle - PGNM (CNRS/Inserm/Université Claude Bernard)
Institut NeuroMyoGene
Faculté de Médecine - 8 avenue Rockefeller
69008 LYON - FRANCE