Un microscope optique à résolution moléculaire
Fruit de la collaboration entre physiciens, mathématiciens et biologistes, un prototype de microscope photonique a été développé. Basé sur la technique « Multi-Angle-TIRF », cet instrument en a repoussé les limites techniques. Il permet d’observer et de mesurer des processus avec une résolution axiale d’environ 30nm et est compatible avec des échantillons vivants ouvrant donc de nombreuses perspectives pour l’imagerie en culture cellulaire.
La microscopie optique est un outil majeur en biologie afin d’observer les échantillons et essayer de comprendre les phénomènes qui s’y déroulent. Mais malgré l'obtention d'instruments toujours plus résolutifs, il existe une limite théorique à leur résolution (la « limite de diffraction » établie en 1873 par Ernst Abbe) que les instruments parvenaient à frôler.
A partir des années 80, des techniques dites de « Super-résolution » (StED, PALM/StORM ou SIM) ont vu le jour pour dépasser (ou plutôt « contourner ») cette limite de diffraction. Ces différentes techniques ont continuement évoluées, avec l’énorme avantage d’être aujourd’hui très résolutives tant en résolution latérale (jusque 20nm, la résolution sur une image) que axiale (jusque 100nm, la résolution pour la 3D). Malheureusement, cela implique d’envoyer énormément d’énergie sur l’échantillon qui doit avoir des marqueurs fluorescents bien particuliers, rendant son utilisation difficile pour certaines applications utilisant des échantillons vivants.
Mais pour un certain nombre d’applications il est plus crucial de pouvoir gagner en résolution axiale, de regarder simultanément plusieurs molécules avec des molécules fluorescentes standard ou des protéines directement fluorescentes. C’est dans ce cadre que la méthode de MA-TIRF (Fluorescence par Réflexion Total Interne à Angle Multiple) peut être un outil particulièrement adapté. Initiée dans les années 90, cette technique utilise une propriété de la lumière, « l’onde évanescente ». Une onde évanescente ne va pénétrer un échantillon que sur quelques centaines de nm lorsqu’on l’illumine avec une source lumineuse très oblique (c’est le principe du TIRF classique). En jouant sur l’angle d’illumination, on va pouvoir faire varier sa pénétration, et c’est donc en combinant précisément plusieurs angles d’illumination que l’on va pouvoir obtenir des informations complémentaires. Mais cela nécessite un algorithme de reconstruction très particulier.
Le prototype qui a été développé atteint une résolution 15 fois supérieure à l’optique. Fruit d'une collaboration entre biologistes, physiciens et mathématiciens, le prototype de microscope et l'algorithme de reconstruction associé permettent d’observer en 3D des cellules avec une résolution axiale de 30nm tout en étant compatible avec trois marquage simultanément et l'observation d’échantillons vivants, ouvrant des perspectives d’imagerie à très haute résolution.
La précision de ce microscope permet de reconstruire des échantillons jusqu'à quasiment 500nm d’épaisseur et de mesurer un décalage extrêmement faible entre 2 marquages équivalents sur une même cellule. Enfin, en plus de permettre de gagner en résolution axiale, son algorithme améliore également la résolution latérale en intégrant un processus de déconvolution.
Utilisant ce prototype, les chercheurs ont voulu mieux comprendre comment des cellules créent et interagissent avec leur environnement direct (la « matrice extra-cellulaire »). En étudiant des intégrines (ancres moléculaires permettant à la cellule de s’accrocher à sa matrice) et des molécules associées, ils ont pu montrer les performances de l’instrument en confirmant l’orientation de cette ancre moléculaire mais aussi en mesurant sa longueur (environ 70nm). La résolution de l'appareil a également permis de dissocier la part d’intégrines véritablement liée à la membrane cellulaire de celle qui est dans des vésicules à l’intérieur de la cellule et d'observer l’épaississement de la matrice. Ces résultats ouvrent la voie à des études à très haute résolution d'un grand nombre de processus biologiques, notamment à proximité de la membrane de la cellule.
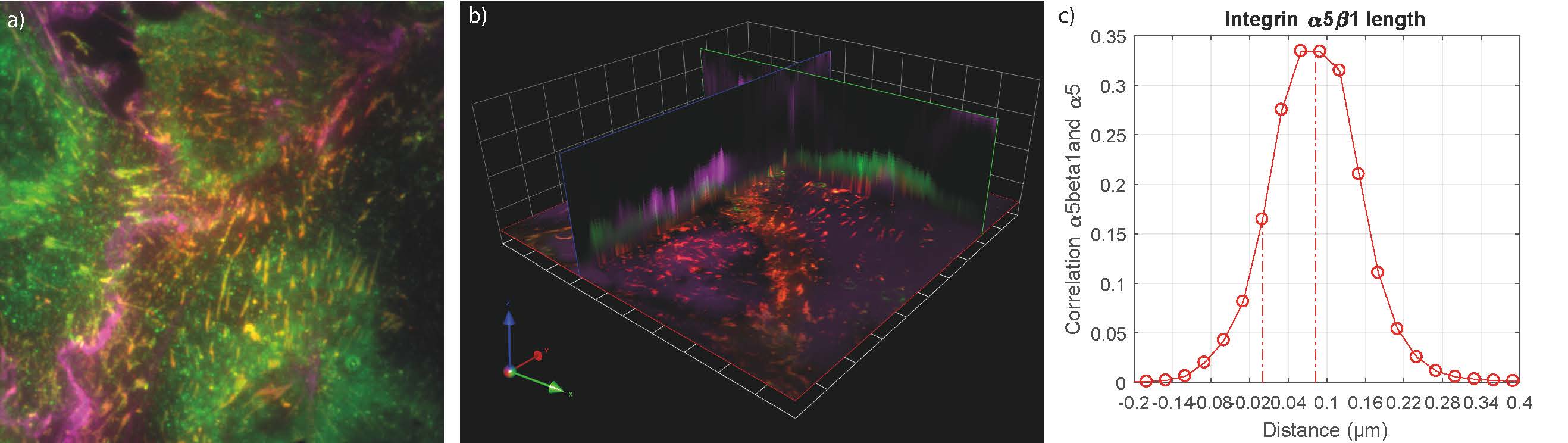
© Sebastien Schaub
En savoir plus
-
Nanometric axial resolution of fibronectin assembly units achieved with an efficient reconstruction approach for multi-angle-TIRF microscopy.
Soubies E, Radwanska A, Grall D, Blanc-Féraud L, Van Obberghen-Schilling E, Schaub E
Scientific Reports 2019 Feb 13 /doi.org/10.1038/s41598-018-36119-3