STORIES, une approche pour cartographier les trajectoires cellulaires dans le temps et l’espace
Dans un article publié dans Nature Methods, des scientifiques présentent STORIES, une nouvelle méthode qui permet de suivre l’évolution des cellules sans avoir besoin de les observer en continu. Cette approche permet de modéliser la différenciation au cours du temps, d’identifier des trajectoires cohérentes dans le cadre du développement ou de la régénération.
Le défi : suivre l’évolution des cellules sans les observer en continu
Comprendre comment des cellules souches pluripotentes individuelles se différencient en plusieurs types cellulaires est un défi fondamental en biologie. Les technologies actuelles apportent des informations précieuses mais limitées.
Le séquençage unicellulaire permet de mesurer, pour chaque cellule isolée, quels gènes sont activés ou silencieux. Il offre donc une vision très fine de l’état d’une cellule, mais uniquement à un instant donné : chaque cellule n’est mesurée qu’une seule fois, sans possibilité d’en suivre directement l’évolution.
La transcriptomique spatiale, quant à elle, cartographie l’expression des gènes directement dans le tissu, en préservant l’emplacement exact de chaque cellule. Elle permet ainsi d’étudier l’influence de l’environnement local (les cellules voisines, la position dans l’organe) mais elle souffre de la même limitation temporelle : chaque coupe tissulaire représente un instant figé.
Aligner plusieurs coupes prélevées à différents moments est en outre particulièrement difficile, en raison des changements de forme du tissu au cours du développement ou de la régénération. Ces contraintes ont freiné la création de cartes spatiotemporelles fiables, pourtant essentielles pour comprendre des processus comme la formation d’un organe ou l’apparition d’un cancer.
La solution : STORIES, une méthode mathématique et spatiale pour reconstruire les trajectoires cellulaires
Pour surmonter ces limites, dans un article publié dans la revue Nature Methods, des scientifiques ont développé STORIES, une approche fondée sur le Transport Optimal, un cadre mathématique utilisé pour comparer de manière cohérente deux ensembles de données. L’idée est de traiter les cellules observées à différents instants comme des distributions à aligner pour en déduire leur évolution probable.
STORIES repose sur une variante avancée de ce cadre, le Fused Gromov-Wasserstein (FGW), qui compare simultanément :
- L’expression génique,
- La position spatiale des cellules.
FGW agit comme une perte d’apprentissage qui permet d’entraîner un modèle apprenant un potentiel de différenciation : un relief abstrait décrivant la manière dont les cellules progressent au fil du temps vers leurs futurs états.
Des performances validées sur plusieurs organismes
Pour évaluer STORIES, les scientifiques ont testé sa capacité à prédire l’expression génique de cellules observées à des temps futurs non utilisés lors de l’entraînement. Trois ensembles de données spatiotemporelles ont été mobilisés :
- développement de la souris,
- développement du poisson-zèbre,
- régénération de l’axolotl.
Dans chaque cas, STORIES surpasse les modèles ne tenant pas compte de l’information spatiale, démontrant que le contexte tissulaire améliore nettement la prédiction de la dynamique cellulaire.
Etudes de cas : gliogenèse et régénération
Deux applications biologiques illustrent la portée de cette méthode.
- Gliogenèse chez la souris
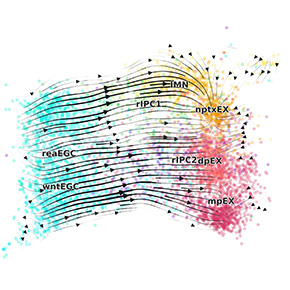
STORIES reconstitue des trajectoires cohérentes avec les étapes connues du développement glial, retrouvant notamment des tendances d’expression telles que celles du gène Aldh1l1, un marqueur de la différenciation astrocytaire, et révélant des motifs de différenciation liés à l’organisation spatiale du tissu. - Régénération de la moelle épinière chez l’axolotl
Le modèle identifie des marqueurs de régénération neuronale comme Nptx1, et met en lumière Rest comme régulateur potentiel supplémentaire du processus de différenciation.
Ces résultats illustrent la capacité de STORIES à générer des trajectoires biologiquement pertinentes en intégrant à la fois l’espace, le temps et l’expression génique.
Enjeux et perspectives
En apprenant un potentiel de différenciation informé par le contexte spatial, STORIES constitue une nouvelle approche puissante pour analyser la dynamique des tissus. Elle éclaire la manière dont les environnements locaux influencent le destin cellulaire, un enjeu majeur en biologie du développement et pour l’étude des premières phases des pathologies.
L’outil, mis à disposition de la communauté scientifique, permettra d’exploiter plus largement des jeux de données existants ou futurs, renforçant l’étude de la biologie unicellulaire.
Cependant, STORIES ne prédit pas encore les positions futures des cellules dans le tissu et ne modélise pas les interactions complexes ou les rétroactions issues du tissu. Étendre la méthode pour intégrer explicitement les dynamiques spatiales et les interactions cellule–cellule sera la prochaine étape vers une véritable reconstruction 4D des tissus biologiques.
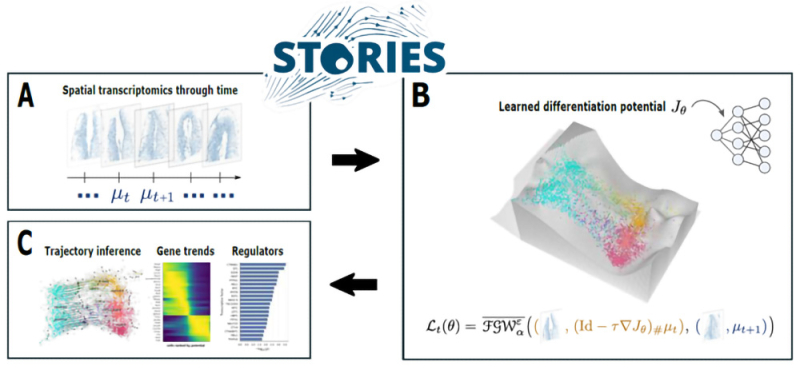
Légende : Vue d’ensemble de STORIES.
a. STORIES est une méthode computationnelle qui prend en entrée des données de transcriptomique spatiale profilées à plusieurs points temporels (𝜇𝑡).
b. STORIES apprend un potentiel de différenciation (𝐽𝜃) paramétré par un réseau neuronal, en minimisant une perte de type Fused Gromov–Wasserstein (ℒ𝑡(𝜃)) qui intègre à la fois les profils d’expression génique et les coordonnées spatiales.
c. Le gradient de ce potentiel peut ensuite être utilisé dans des analyses en aval pour inférer les vitesses cellulaires, reconstruire des trajectoires et identifier des dynamiques d’expression génique ainsi que des régulateurs potentiels.
En savoir plus : Huizing GJ, Samaran J, Capocefalo D, Audit A, Peyré G, Cantini L. STORIES: learning cell fate landscapes from spatial transcriptomics using optimal transport. Nat Methods. 2025 Nov 3. doi: 10.1038/s41592-025-02855-4. Epub ahead of print. PMID: 41184554.
Contact
Laboratoires
- Département biologie du développement et cellules souches (CNRS/Institut Pasteur)
Institut Pasteur 25 rue du Dr Roux,
75015 Paris - Département de mathématiques et applications de l’ENS Paris - DMA (CNRS/ENS Paris)
45, rue d'Ulm,
75005 Paris