Le vol de coiffe, une stratégie clé des virus grippaux
Pour fabriquer des ARN viraux efficaces et non reconnus par les défenses de la cellule, les virus grippaux volent la « coiffe » protectrice de certains ARN cellulaires. Une étude publiée dans la revue Nature décrit en détail comment les virus réalisent ce piratage moléculaire, ouvrant de nouvelles pistes pour le développement d’antiviraux.
Vol de coiffe
Les virus grippaux possèdent un génome constitué d’ARN simple brin. Après avoir introduit leur matériel génétique dans la cellule hôte, ils en exploitent les composants et machineries moléculaires pour produire de nouvelles particules virales. En dérobant la coiffe de certains ARN de la cellule, ils favorisent leur propre multiplication tout en contournant certains mécanismes de défense cellulaire.
Ce processus, appelé « vol de coiffe », repose sur l’activité coordonnée de deux machineries de « recopiage » : la polymérase virale et l’ARN polymérase II (Pol II) cellulaire. La Pol II transcrit l’ADN nucléaire en ARN, notamment en ARN messagers (ARNm). Dès le début de leur synthèse par la Pol II, les ARN acquièrent à leur extrémité 5’ une coiffe chimique, indispensable à leur stabilité, à leur traduction et à leur reconnaissance comme ARN du « soi » par le système immunitaire. En l’absence de coiffe, un ARN est perçu comme étranger et déclenche une réponse antivirale.
La plupart des virus disposent d’une polymérase capable d’ajouter elle-même une coiffe aux ARNm viraux, mais ce n’est pas le cas des virus grippaux. Leur polymérase (FluPol) a évolué vers un mécanisme original de « vol de coiffe », permettant la synthèse d’ARNm viraux coiffés, fonctionnels et indétectables par le système immunitaire, au détriment de la synthèse des ARN coiffés de la cellule hôte.
Un vol en trois étapes
Bien que l’interaction physique entre la FluPol et la Pol II cellulaire ait été établie, le mécanisme précis du vol de coiffe restait mystérieux. Dans un article publié dans la revue Nature, une collaboration scientifique internationale entre trois équipes a réussi à l’élucider.
Le processus de vol de coiffe a été reconstitué in vitro en présence des polymérases purifiées, puis visualisé par cryo-microscopie électronique à résolution quasi-atomique.
Trois étapes principales ont été identifiées :
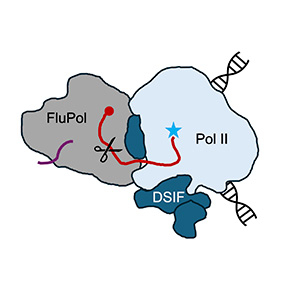
- la FluPol se lie à la Pol II cellulaire peu après l’ajout de la coiffe à l’extrémité d’un ARN naissant ;
- grâce à son activité endonucléase, elle clive l’ARN naissant en aval de la coiffe ;
- le court fragment d’ARN coiffé ainsi généré est réorienté vers le site actif de la FluPol, s’hybride à l’extrémité de l’ARN génomique viral, et sert d’amorce pour la synthèse d’un ARNm viral coiffé.
Un facteur régulateur associé à la Pol II cellulaire, appelé DSIF, joue également un rôle essentiel à l’interface avec la FluPol.
L’interface FluPol – Pol II, une cible potentielle pour de nouveaux antiviraux
Ces travaux permettent d’élucider une étape clé de la multiplication d’un virus ayant un impact majeur en santé humaine et animale. Des expériences de mutagénèse montrent que l’altération des sites d’interaction entre la FluPol et le complexe cellulaire Pol II-DSIF réduit fortement l’activité de la FluPol, aussi bien in vitro que dans des cellules vivantes.
Les interfaces d’interaction entre les polymérases virale et cellulaire apparaissent ainsi comme des cibles potentielles pour le développement de nouveaux composés antiviraux, ouvrant la voie à des stratégies thérapeutiques originales contre les infections grippales.
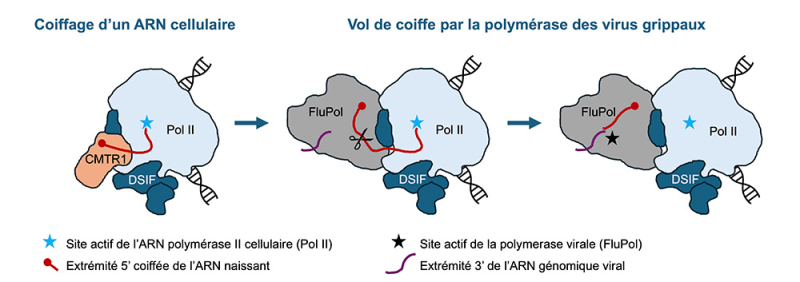
Figure : Modèle du mécanisme de vol de coiffe par la polymérase des virus grippaux (FluPol), issu de la caractérisation structurale et fonctionnelle du complexe FluPol-Pol II. Des enzymes cellulaires, notamment CMTR1, ajoutent une coiffe chimique à l’extrémité 5’ des ARN en cours de synthèse par l’ARN polymérase II cellulaire (Pol II). L’enzyme CMTR1 se dissocie de la Pol II, qui forme alors avec le facteur cellulaire DSIF un complexe transcriptionnel dit « d’élongation ». La FluPol s’associe à ce complexe et clive l’ARN naissant en aval de la coiffe. Le court fragment d’ARN coiffé résultant de ce clivage est réorienté vers le site actif de la FluPol, s’hybride à l’extrémité 3’ de l’ARN génomique viral, et est utilisé comme amorce pour recopier l’ARN génomique viral en un ARNm viral coiffé.
En savoir plus : Rotsch AH, Li D, Dupont M, Krischuns T, Neef U, Oberthür C, Stelfox A, Lukarska M, Fianu I, Lidschreiber M, Naffakh N, Dienemann C, Cusack S, Cramer P. Mechanism of co-transcriptional cap snatching by influenza polymerase. Nature. 2026 Mar 4. doi: 10.1038/s41586-026-10189-0. Epub ahead of print. PMID: 41781612.
Contact
Laboratoire
- Virologie (CNRS/Institut Pasteur)
Institut Pasteur
25-28 rue du Dr Roux,
75015 Paris - EMBL Grenoble
71 Avenue des Martyrs,
38042 Grenoble