Girdin : une protéine clé du remodelage tissulaire en trois dimensions
Comprendre comment les cellules se réorganisent pour former des tissus et des organes fonctionnels est essentiel pour décrypter la morphogenèse et certains processus pathologiques comme la progression tumorale. Une étude publiée dans la revue Development met en évidence le rôle central de la protéine Girdin dans le remodelage des jonctions d’adhésion entre cellules lors de leur réorganisation en trois dimensions.
Comprendre la réorganisation des cellules dans les tissus
La morphogenèse, c’est-à-dire la formation et l’organisation des tissus au cours du développement, repose sur des mouvements cellulaires coordonnés. Ces mouvements sont contrôlés par l’interaction entre le cytosquelette d’actine, un réseau de filaments qui donne sa forme à la cellule et génère des forces mécaniques, et les jonctions adhérentes, des structures moléculaires qui relient les cellules entre elles.
Certaines protéines jouent un rôle clé dans ces jonctions soumises à tension mécanique. Parmi elles figurent Vinculin et LIM-Ajuba, capables de détecter les forces exercées sur les jonctions, ainsi que Myosine II, un moteur moléculaire qui permet la contraction du réseau d’actine. Pourtant, l’inactivation de ces protéines ne provoque parfois que des effets limités, suggérant l’existence de mécanismes compensatoires et d’autres acteurs impliqués dans la régulation de l’adhésion cellulaire.
Un modèle original pour étudier la morphogenèse en 3D
Pour mieux comprendre ces mécanismes, les scientifiques ont étudié la formation des branches dorsales de l’appareil respiratoire de l’embryon de drosophile, un modèle pour étudier la formation d’organes dans un organisme en développement. Ce système présente une particularité remarquable : les cellules y réorganisent leur position dans l’épithélium sans division cellulaire et sans intervention de la Myosine II, ce qui en fait un modèle idéal pour analyser d’autres mécanismes de remodelage tissulaire.
Les résultats, publiés dans la revue Development, montrent que les jonctions adhérentes de ces cellules possèdent une composition inhabituelle : elles ne contiennent ni Vinculine ni LIM-Ajuba, mais sont au contraire riches en Girdin, une protéine adaptatrice du cytosquelette conservée de la drosophile à l’être humain et déjà impliquée dans la progression tumorale.
Un nouvel outil génétique pour dépolymériser l’actine
Au cours de cette étude, les scientifiques ont également développé un outil génétique inédit permettant de dépolymériser l’actine directement dans les cellules vivantes avec une résolution cellulaire.
Cette approche constitue une alternative aux méthodes pharmacologiques classiques, souvent peu spécifiques et difficilement efficaces dans des tissus entiers. Elle permet ainsi d’étudier de manière plus précise le rôle du cytosquelette d’actine dans la morphogenèse.
Girdin, un acteur central de l’intercalation cellulaire
Les résultats de l’étude montrent que la protéine Girdin joue un rôle déterminant dans la réorganisation des cellules au sein du tissu :
- elle est indispensable au maintien d’un rythme normal d’intercalation cellulaire en trois dimensions, un processus par lequel les cellules changent de position les unes par rapport aux autres ;
- elle organise le réseau d’actine apical associé aux jonctions adhérentes ;
- contrairement à Vinculin et LIM-Ajuba, Girdin apparaît comme un composant structurel du complexe des jonctions adhérentes.
Ces travaux révèlent ainsi un mécanisme de remodelage des jonctions adhérentes indépendant des protéines mécano-sensibles classiques et de la Myosine II.
Associé au nouvel outil génétique développé par les scientifiques, ce résultat ouvre de nouvelles perspectives pour décrypter, à l’échelle moléculaire, les mécanismes encore mal compris qui gouvernent la réorganisation des tissus en trois dimensions, des processus essentiels au développement embryonnaire mais aussi impliqués dans certaines pathologies, notamment les cancers.
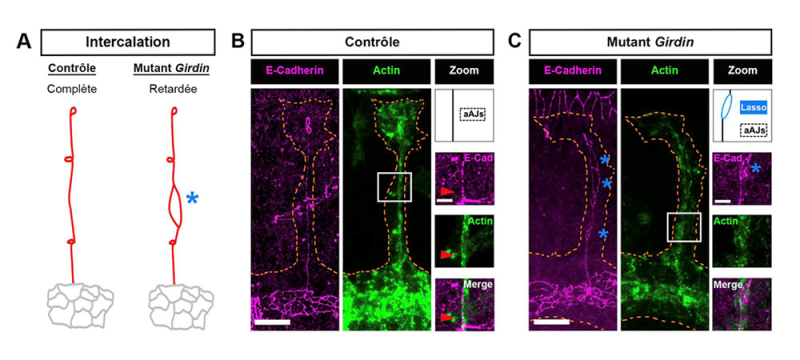
Figure : Girdin est nécessaire à l’intercalation cellulaire en 3D et à l'enrichissement en actine au niveau des jonctions adhérentes dans les branches dorsales de l’appareil respiratoire embryonnaire de drosophile. (A) Organisation des jonctions adhérentes (JA) dans une branche dorsale de l’appareil respiratoire de l’embryon de drosophile. L’intercalation est complète en condition contrôle et retardée dans une branche mutante pour Girdin, révélée par la formation d’un lasso (étoile bleue). (B) Distribution de l’actine par rapport aux JA (E-Cadherin) dans une branche dorsale témoin et une branche dorsale mutante pour Girdin. Les pointillés orange délimitent les contours des branches. Les agrandissements de la région encadrée en blanc montrent une organisation linéaire continue des JA dans la branche témoin, contrastant avec une organisation discontinue en « lasso » dans la branche mutante pour Girdin (étoiles bleues et voir schémas), associée à une forte diminution de l’actine aux jonctions. Les flèches rouges indiquent les JA. Barre d’échelle : 10 μm.
En savoir plus : Carvalho S, Laprise P, Guichet A, Brodu V. Girdin controls the pace of 3D tracheal cell intercalation by coupling adherens junctions to the actin cytoskeleton in Drosophila. Development. 2026 Feb 1;153(3):dev205073. doi: 10.1242/dev.205073. Epub 2026 Feb 11. PMID: 41537258.
Contact
Laboratoire
Institut Jacques Monod – IJM (CNRS/Université Paris Cité)
Bât.Buffon - 15 rue Hélène Brion
75205 Paris