Fluidité intracellulaire et pouvoir infectieux du champignon Candida albicans
Dans un article publié dans la revue Nature Microbiology, des scientifiques mettent en évidence un mécanisme jusque-là inconnu chez Candida albicans, un champignon opportuniste responsable d’infections graves chez l’homme, en particulier chez les patients immunodéprimés. Ils montrent que, lorsqu’il adopte une forme invasive, l’intérieur de ses cellules devient plus fluide, un phénomène lié à une diminution du nombre de ribosomes. Cette découverte ouvre de nouvelles pistes pour limiter sa capacité infectieuse.
Candida albicans, un champignon pathogène opportuniste sous haute surveillance
Candida albicans est un champignon microscopique naturellement présent chez l’être humain. Il est en général inoffensif, mais peut provoquer des infections parfois graves chez les personnes dont le système immunitaire est affaibli : on parle alors de champignon pathogène opportuniste. En raison de son importance en santé publique, il figure parmi les agents fongiques jugés prioritaires par l’Organisation mondiale de la Santé.
Une caractéristique clé de ce champignon est sa capacité à changer de forme. Il peut passer d’une forme ovale à une forme allongée filamenteuse, mieux adaptée pour adhérer aux tissus et les envahir, ce qui favorise l’infection.
Le cytoplasme du champignon, un élément peu étudié
Si de nombreuses recherches se sont intéressées aux changements intracellulaires accompagnant cette transition de forme, le rôle du cytoplasme (le milieu visqueux et très encombré qui remplit la cellule) restait peu exploré. Or, ce compartiment est le siège de réactions chimiques et de formations de complexes moléculaires essentielles à la vie cellulaire. En effet, il a été démontré que l'encombrement cytoplasmique affecte de manière critique la diffusion des protéines, de l'ARN et des organites dans le cytoplasme.
Parmi les principaux contributeurs à cet encombrement figurent les ribosomes, de grandes machines moléculaires chargées de fabriquer les protéines. Très abondants, ils consomment aussi une part importante de l’énergie cellulaire.
Des sondes micro rhéologiques pour mesurer la fluidité cellulaire
Pour comprendre comment le cytoplasme évolue lorsque Candida albicans change de forme, les scientifiques, dans un article publié dans la revue Nature Microbiology, ont combiné plusieurs disciplines, de la biologie cellulaire à la biophysique, en passant par la modélisation et l’imagerie de pointe.
Ils ont notamment utilisé des sondes micro rhéologiques : de minuscules particules fluorescentes, appelées GEMs (Genetically Encoded Multimeric nanoparticles), exprimées directement dans les cellules. En suivant les déplacements de ces sondes au fil du temps, les scientifiques ont pu mesurer localement les propriétés mécaniques du cytoplasme, comme sa fluidité.
Ces mesures révèlent que, lorsque le champignon adopte une forme filamenteuse, le cytoplasme devient progressivement plus fluide. Plus les filaments s’allongent, moins le cytoplasme est encombré.
La baisse du nombre de ribosomes au cœur du mécanisme
En combinant simulations, analyses globales des protéines et observations directes par cryo-microscopie électronique, les chercheurs ont montré que cette augmentation de fluidité est liée à une diminution de la concentration en ribosomes.
Ils observent une baisse spécifique des protéines constituant les ribosomes ainsi qu’un nombre réduit de ces complexes dans les cellules filamenteuses. De manière remarquable, bloquer la fabrication des ribosomes suffit à déclencher le changement de forme du champignon, montrant que ce mécanisme joue un rôle critique dans la morphogenèse.
Cette étude met en lumière une stratégie d’adaptation originale de Candida albicans : en rendant son cytoplasme plus fluide, le champignon facilite sa transformation en une forme favorisant l’invasion des tissus. Elle suggère également des pistes thérapeutiques inédites : en ciblant les éléments qui contrôlent la fabrication des protéines, il serait possible de bloquer le changement de morphologie de ce champignon et donc de limiter sa capacité infectieuse. Ces résultats ouvrent la voie à de nouvelles stratégies combinées pour lutter plus efficacement contre les infections fongiques, un enjeu croissant de santé publique.
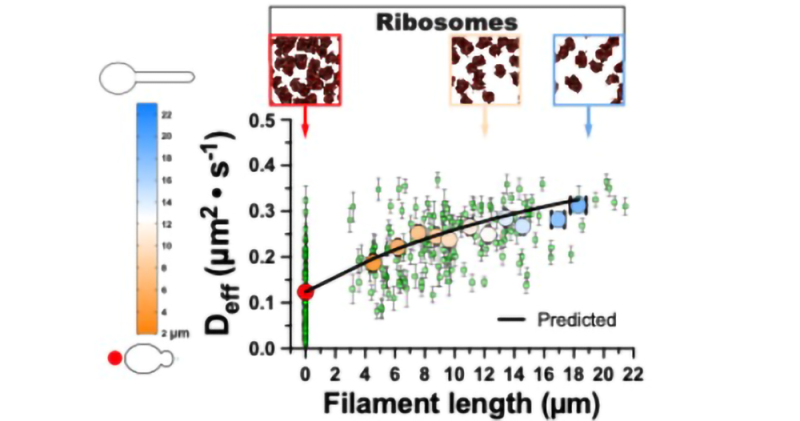
Figure : La diffusion des macromolécules (Deff) dans la cellule de C. albicans augmente avec l’extension du filament. Les symboles du graphe représentent des cellules individuelles (petits carrés) ou des groupes de cellules (grands cercles), les couleurs correspondent aux longueurs de filament. Les images au-dessus du graphe montrent l'encombrement des ribosomes, qui diminue à mesure que le filament s'allonge.
En savoir plus : Serrano A, Puerner C, Chevalier L, Plumb E, Elferich J, Diggs S, Sinn LR, Grigorieff N, Ralser M, Delarue M, Bassilana M, Arkowitz RA. Decreased cytoplasmic crowding via inhibition of ribosome biogenesis can trigger Candida albicans filamentous growth. Nat Microbiol. 2026 Jan;11(1):169-179. doi: 10.1038/s41564-025-02205-2. Epub 2025 Dec 10. PMID: 41372638.
Fluidité intracellulaire et pouvoir infectieux du champignon Candida albicans
Diffusion dans le cytoplasme des sondes micro rhéologiques passives de 40 nm.
© Antonio Serrano & Robert Arkowitz
Audiodescription
Contact
Laboratoire
Institut de biologie Valrose (iBV) (CNRS / Inserm / Université Côte d'Azur)
Université Côte d'Azur
06108 Nice Cedex