Douleur neuropathique : les limites des prédictions de la pharmacologie cellulaire
La douleur neuropathique, conséquence d’une atteinte du système somatosensoriel, concerne jusqu’à 8 % de la population et demeure difficile à traiter. Une étude publiée dans The British Journal of Pharmacology montre que la caractérisation pharmacologique des récepteurs opioïdes, même dans leur environnement natif, ne permet pas de prédire de manière fiable l’efficacité analgésique in vivo, en particulier en conditions neuropathiques.
Des traitements imparfaits face à la douleur neuropathique
Les traitements de première intention de la douleur neuropathique reposent principalement sur l’utilisation d’antidépresseurs ou d’anticonvulsivants, dont l’efficacité ne concerne qu’environ 60 % des patients. Les stratégies alternatives font appel à des opioïdes ciblant les récepteurs opioïdes μ, mais leur efficacité demeure limitée. Elles sont en outre associées à des effets indésirables importants, tels que la tolérance (qui impose une augmentation progressive des doses pour maintenir l’effet analgésique) et le risque de dépendance. Dans ce contexte, le développement de nouveaux analgésiques ou l’identification de cibles thérapeutiques innovantes constituent un enjeu primordial.
L’un des défis majeurs en pharmacologie est la capacité à prédire des effets comportementaux sur la base des affinités et sélectivités des ligands pour les récepteurs et de leur aptitude à activer différentes voies de signalisation. L'expression induite de récepteurs dans des cellules qui ne les produisent pas naturellement est largement utilisée pour étudier ces propriétés. Toutefois, la composition cellulaire et les niveaux d'expression des récepteurs influencent l'efficacité des ligands. Les différences dans le contenu cellulaire peuvent ainsi générer un biais de signalisation spécifique à la cellule rendant l’extrapolation des données issues de ces systèmes peu fiables.
Hétéromères opioïdes μ–δ : une cible prometteuse mais complexe
Les récepteurs opioïdes appartiennent à la famille des récepteurs couplés aux protéines G. Les récepteurs opioïdes μ et δ modulent les seuils de détection thermique et mécanique et sont largement distribués dans les circuits de la douleur. Lorsqu’ils sont co-exprimés dans un même neurone, ils peuvent interagir pour former une nouvelle entité appelée hétéromère μ–δ. Ces hétéromères présentent des propriétés spécifiques en termes de liaison des ligands, de signalisation cellulaire et de trafic intracellulaire.
La présence d’hétéromères μ–δ dans les ganglions de la racine dorsale, la moelle épinière et des régions du cerveau impliquées dans la douleur en fait une cible thérapeutique potentielle. Leur activation induit un effet analgésique chez des animaux naïfs. Dans ce contexte, les propriétés de deux ligands ciblant spécifiquement ces hétéromères, le CYM51010 et le MP135, ont été caractérisées et comparées à celles de la morphine, ligand opioïde de référence ciblant le récepteur μ. Les résultats ont été publiés dans la revue The British Journal of Pharmacology.
L’affinité de ces trois composés pour les récepteurs opioïdes μ et δ a été mesurée sur des tissus cérébraux de souris. Leur capacité à activer les voies de signalisation dépendantes des protéines G ou de la β-arrestine a été évaluée dans des cultures de cellules primaires. Les scientifiques ont ensuite examiné dans quelle mesure ces propriétés permettaient de prédire la réponse comportementale, en comparant l’efficacité analgésique des ligands chez des souris naïves et neuropathiques.
Des profils cellulaires similaires mais des réponses comportementales différentes
Les trois composés présentent des profils de liaison comparables et activent de manière similaire les voies dépendantes des protéines G. L’utilisation de souris déficientes pour l’un des deux récepteurs (souris knock-out μ ou knock-out δ) montre que ces trois ligands sont peu sélectifs et capables d’activer la cascade de signalisation dépendante des protéines G en se liant aux récepteurs μ ou δ associés ou non.
Les trois composés induisent une analgésie thermique comparable chez les souris naïves, bien que l’efficacité et la durée soient réduites chez les femelles. Ceci est vraisemblablement lié à une métabolisation plus active des composés chez ces dernières. L’utilisation de souris knock-out dépourvues de l’un des deux récepteurs a montré que l’effet analgésique des trois ligands dépend de la présence du récepteur μ, en accord avec les observations réalisées en modèles cellulaires. En revanche, le récepteur δ semble peu ou pas impliqué, bien que les trois composés soient capables de l’activer efficacement.
L’effet comportemental des composés a ensuite été évalué en conditions neuropathiques, à l’aide d’un modèle murin dans lequel deux branches du nerf sciatique sont ligaturées et sectionnées. Malgré des profils pharmacologiques similaires au niveau cellulaire, un seul des deux ligands ciblant les hétéromères μ–δ, le CYM51010, produit un effet analgésique en augmentant le seuil mécanique. Cet effet nécessite l’activation conjointe des récepteurs μ et δ, indiquant une modification du profil fonctionnel dans ce contexte pathologique.
L’ensemble de ces résultats montre que la caractérisation pharmacologique des récepteurs endogènes ne suffit pas pour prédire de manière fiable la réponse analgésique, en particulier en conditions neuropathiques. Ils soulignent la complexité des mécanismes impliqués à l’échelle de l’organisme entier et la nécessité de considérer les modifications dynamiques de la distribution des récepteurs cibles et/ou du recâblage des circuits neuronaux associés aux états douloureux chroniques. Ces éléments sont cruciaux pour compléter le caractère prédictif limité des données cellulaires et améliorer l’efficacité clinique des médicaments en cours de développement.
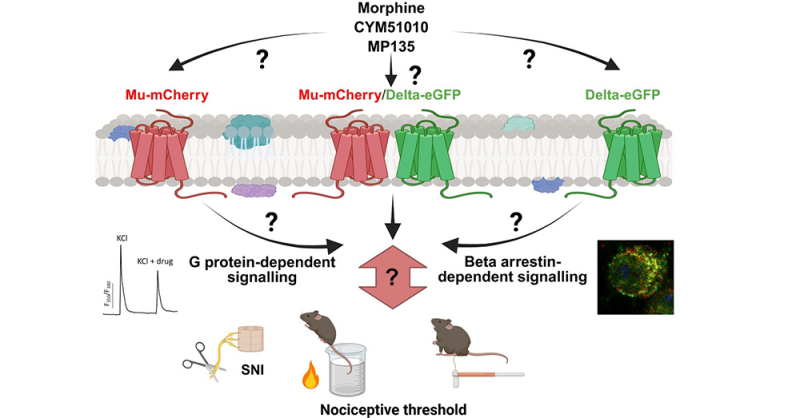
Figure : L’un des défis majeurs en pharmacologie est de prédire les effets comportementaux d’une molécule sur la base de données collectées au niveau cellulaire. Dans ce contexte, la caractérisation pharmacologique de composés opioïdes a été réalisée au niveau cellulaire à l’aide de récepteurs opioïdes dans leur environnement natif et la réponse analgésique a été évaluée chez des souris douloureuses en condition neuropathique.
En savoir plus : Inquimbert P, Fitterer C, Hugel S, Jesic M, Goumon Y, Andry V, Schneider S, Daubeuf F, Faouzi A, Doridot S, Majumdar S, Bihel F, Schmitt M, Massotte D. Divergence in μ and δ opioid receptor pharmacology in neurons and antinociceptive efficacy in neuropathic pain: Insights from MP135 and CYM51010. Br J Pharmacol. 2026 Jan 6. doi: 10.1111/bph.70285. Epub ahead of print. PMID: 41492212.
Contact
Laboratoire
Institut des neurosciences cellulaires et intégratives - INCI (CNRS)
8 allée du général de Rouvillois,
67000 Strasbourg
