Un mécanisme inédit régulant le cycle cellulaire chez les plantes : le rôle clé de la protéine FBL17
Le contrôle précis du cycle cellulaire est essentiel pour assurer la stabilité du génome. Dans Science Advances, des scientifiques montrent que la protéine FBL17 agit comme un régulateur clé du cycle cellulaire chez Arabidopsis thaliana. En contrôlant la stabilité de facteurs transcriptionnels du module RBR1–E2F/DP, elle prévient une activation excessive des gènes du cycle cellulaire et de la réponse aux dommages à l’ADN, contribuant ainsi au maintien de l’intégrité du génome.
Régulation du cycle cellulaire chez les plantes
Chez tous les organismes eucaryotes, la progression du cycle cellulaire repose sur une régulation fine de l’expression et de la stabilité de nombreuses protéines clés. Chez les plantes, ce contrôle est particulièrement crucial pour coordonner division cellulaire, différenciation et maintien de l’intégrité du génome.
Dans une étude publiée dans Science Advances, des scientifiques ont étudié la protéine FBL17, une protéine F-box chez Arabidopsis thaliana, plante modèle en biologie végétale. Les protéines F-box participent au système d’ubiquitination, un mécanisme cellulaire qui marque certaines protéines pour entraîner leur dégradation sélective.
FBL17 était connue pour être indispensable à la progression du cycle cellulaire. Toutefois, ses mécanismes d’action restaient mal compris. Les plantes mutantes dépourvues de FBL17 présentent en effet de graves défauts de développement, associés à une dérégulation massive de gènes impliqués dans le cycle cellulaire et la réponse aux dommages à l’ADN.
FBL17 cible le module RBR1-E2F/DP
Pour comprendre ce rôle, les scientifiques ont combiné des approches génétiques, biochimiques et génomiques : interactomique par spectrométrie de masse, analyses transcriptomiques et ChIP-seq.
Leurs résultats montrent que FBL17 interagit directement avec plusieurs composants du module transcriptionnel RBR1–E2F/DP, un système central de contrôle du cycle cellulaire. Ce module régule l’expression de nombreux gènes nécessaires à la réplication de l’ADN et à l’entrée en phase S.
L’étude révèle que FBL17 régule la stabilité de certains facteurs E2F activateurs. Mais surtout, elle met en évidence que l’accumulation aberrante du répresseur transcriptionnel E2Fc est responsable des défauts sévères observés chez les mutants fbl17.
De manière remarquable, l’inactivation génétique de E2Fc suffit à restaurer en grande partie un développement normal chez les plantes dépourvues de FBL17. Cette suppression s’accompagne d’une normalisation de l’expression de nombreux gènes du cycle cellulaire et de la réponse aux dommages à l’ADN. L’étude montre également qu’en l’absence de FBL17, E2Fc perd sa capacité à se lier à la chromatine et à recruter la protéine RBR1, ce qui conduit à une dérégulation transcriptionnelle profonde.
Ces travaux mettent en évidence un mécanisme inédit par lequel une protéine F-box ajuste finement l’activité transcriptionnelle du module RBR1-E2F afin de garantir la progression normale du cycle cellulaire et d’éviter une activation inappropriée des voies de réponse aux dommages à l’ADN. Plus largement, ils soulignent le rôle central de l’ubiquitination dans l’intégration des signaux contrôlant développement et stabilité du génome chez les plantes.
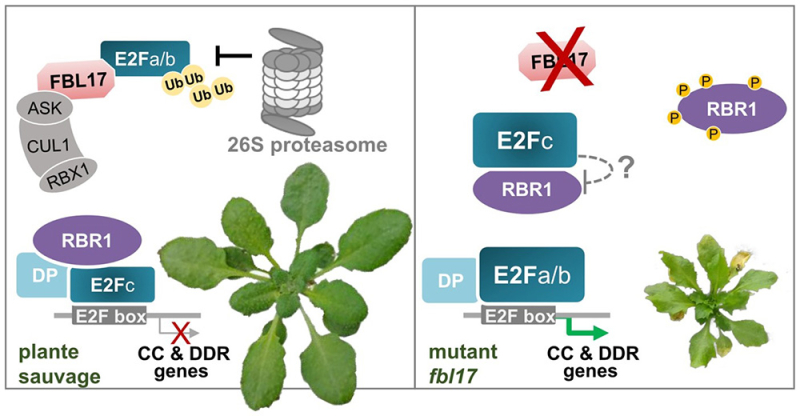
Figure : La protéolyse ubiquitine-dépendante joue un rôle clé dans la coordination de la progression du cycle cellulaire et du maintien de l’intégrité du génome. Chez Arabidopsis thaliana, la protéine F-box FBL17 interagit avec différents composants du module transcriptionnel RBR1-E2F et contribue à la dégradation spécifique des facteurs E2Fa et E2Fb. Chez le mutant fbl17, les trois facteurs de transcription E2F s'accumulent fortement, mais E2Fc ne joue plus son rôle de répresseur, conduisant à l'activation inappropriée des gènes du cycle cellulaire et des voies de réponse aux dommages à l’ADN. De manière remarquable, la mutation du gène E2Fc supprime les altérations développementales et transcriptionnelles sévères observées chez le mutant fbl17. CC, Cell Cycle; DDR, DNA Damage Response.
En savoir plus : Juliette Espanet et al., Tuning of the RBR1-E2F/DP transcriptional module by the F-box protein FBL17.Sci. Adv.12,eadz2439(2026).DOI:10.1126/sciadv.adz2439
Contact
Laboratoire
Institut de biologie moléculaire des plantes - IBMP (CNRS)
12, rue du général Zimmer,
67084 Strasbourg, France
