Comment les gènes de virulence réorganisent le génome de Salmonella
Dans un article publié dans la revue Nature Communications, des scientifiques montrent comment l’activation de gènes de virulence acquis par transfert horizontal chez Salmonella enterica s’accompagne d’un remodelage local et dynamique de la chromatine bactérienne. Ces travaux révèlent un lien étroit entre organisation tridimensionnelle du génome, régulation de l’expression génique et limitation du coût cellulaire associé à la pathogénicité.
Un génome bactérien en perpétuelle réorganisation
La chromatine constitue un cadre universel pour organiser et réguler les génomes dans les trois domaines du vivant. Chez les bactéries, elle est formée d’un ADN fortement surenroulé, associé à de petites protéines liant l’ADN, appelées protéines associées au nucléoïde (NAPs). Leur liaison à l’ADN induit des phénomènes de courbure, de pontage, de revêtement et/ou d’enroulement de l’ADN, générant des architectures chromatiniennes spécifiques.
La chromatine bactérienne peut ainsi adopter un état réprimé (chromatine silencieuse) ou un état activement transcrit (chromatine active). La chromatine silencieuse est majoritairement associée à H-NS, un répresseur xénogénique qui limite l’expression des gènes acquis par transfert horizontal, souvent coûteux pour la cellule. À l’inverse, la chromatine active est fortement occupée par l’ARN polymérase et se caractérise par différents niveaux de surenroulement de l’ADN. Cependant, la transition entre ces deux états et les changements qui l’accompagnent restent encore mal compris.
Isoler les bactéries virulentes pour mieux comprendre leur génome
Dans un article publié dans la revue Nature Communications, des scientifiques se sont intéressés à l’organisation de la chromatine dans des régions acquises horizontalement chez Salmonella enterica sérovar Typhimurium, en particulier l’ilot de pathogénicité 1 (SPl-1). Cet ilot code un système de sécrétion de type III ainsi que des effecteurs nécessaires à l’invasion des cellules épithéliales de l’hôte. Cette étude présentait un défi expérimental, car l’activation de cet îlot ne concerne qu’une faible fraction de la population bactérienne.
Pour surmonter cette difficulté, les scientifiques ont développé une méthode permettant de séparer les bactéries exprimant SPI-1 de celles qui ne l’expriment pas. Cette approche a rendu possible une analyse comparative fine de l’organisation du génome et de la chromatine dans ces deux états fonctionnels distincts.
Un remodelage chromatinien finement contrôlé
Grâce à des approches de génomique fonctionnelle, ils ont montré que l’expression de SPI-1 s’accompagne d’un remodelage local de la chromatine, caractérisé par des modifications profondes de l’organisation tridimensionnelle et de l’occupation protéique. Des techniques de microscopie 3D à haute résolution ont également révélé que cette activation est associée à un repositionnement de SPI-1 vers la périphérie du nucléoïde.
Ces travaux apportent de nouveaux éclairages sur les interactions entre répression xénogénique, mécanismes de contre-répression et architecture de la chromatine bactérienne. Ils mettent en évidence un remodelage chromatinien finement régulé, permettant de limiter le coût cellulaire lié à l’activation des gènes de virulence, et établissent un lien direct entre l’organisation linéaire (1D) du génome et son repliement tridimensionnel (3D), au cœur de l’intégration évolutive de l’ADN acquis.
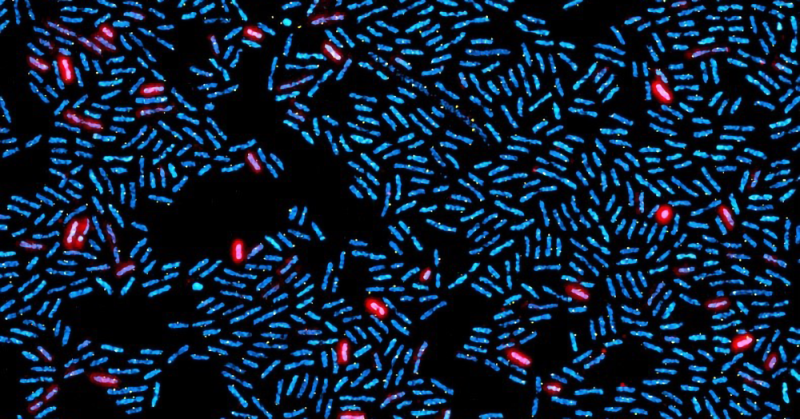
Figure : Champ représentatif de microscopie à illumination structurée (SIM). Les cellules exprimant SPI-1 sont en rouge (mCherry+), les nucléoïdes en cyan, et le locus SPI-1 est visualisé sous la forme d’un foyer jaune.
En savoir plus : Kortebi, M., Bourge, M., Le Bars, R. et al. Bacterial chromatin remodeling associated with transcription-induced domains at pathogenicity Islands. Nat Commun 17, 161 (2026). https://doi.org/10.1038/s41467-025-67746-w
Contact
Laboratoire
Institut de Biologie Intégrative de la Cellule - I2BC (CEA/CNRS/Université Paris-Saclay)
Avenue de la terrasse,
91190 Gif-sur-Yvette