Quand dupliquer le génome redessine sa structure de fontaines en vagues
Dans un article publié dans Genome Biology, des scientifiques montrent que la réplication de l’ADN n’assure pas seulement la duplication fidèle du génome : elle contribue également à remodeler l’organisation tridimensionnelle des chromosomes dans le noyau. Grâce à une approche combinant modélisation biophysique et expériences de biologie moléculaire chez la levure de boulanger, ils révèlent comment les fourches de réplication influencent la structure du génome à plusieurs échelles.
Un modèle 3D du génome pour tester le rôle des fourches de réplication
Avant chaque division cellulaire, l’ADN doit être entièrement dupliqué afin que chaque cellule fille reçoive une copie fidèle du génome. Chez les eucaryotes, cette duplication se produit durant la phase S du cycle cellulaire, et démarre à partir de plusieurs « origines » réparties le long du génome. À chaque origine, deux fourches de réplication, dites « sœurs », partent en sens opposé et dupliquent progressivement l’ADN tout en modifiant la manière dont se plient et s’organisent les chromosomes dans l’espace du noyau cellulaire.
Dans cette étude publiée dans la revue Genome Biology, les scientifiques se sont intéressés à ces effets structurels de la réplication.
Ils ont développé une stratégie interdisciplinaire combinant modélisation biophysique et expériences de biologie moléculaire afin d’explorer l'influence de la réplication sur le repliement des chromosomes chez la levure de boulanger, un organisme modèle souvent utilisé pour ce type d’études.
En intégrant, dans une modélisation numérique, une description réaliste de l'architecture 3D du génome de levure et de la chronologie de sa réplication, ils ont pu tester différentes hypothèses sur le comportement des fourches de réplication et prédire leurs impacts sur l’organisation des chromosomes à plusieurs échelles.
De la fontaine locale à la vague globale : une organisation spatiale orchestrée par la réplication
Leur modèle indique qu’à l’échelle locale, des interactions entre les deux fourches partant d’une même origine doivent laisser une signature bien identifiable dans les données : des « fontaines » de contacts, qui se déploient à partir des origines et correspondent à la formation dynamique de boucles d’ADN guidées par les fourches-sœurs. Grâce à de nouvelles expériences menées dans différentes conditions, ils ont confirmé l’existence de ces fontaines in vivo.
A plus grande échelle, le modèle suggère que la répartition spatiale particulière des origines de réplication dans le noyau de la levure génère une « vague » de réplication qui progresse depuis l’un des pôles du noyau. Enfin, la comparaison entre prédictions et données expérimentales suggère que les différentes paires de fourches-sœurs réplicant le génome en parallèle ne se regroupent pas en « usines » de réplication, dont l’observation antérieure par microscopie pourrait être un artefact dû à la résolution limitée des techniques utilisées.
Pour conclure, les implications de ce travail sont nombreuses. Elles suggèrent que la réplication impacte activement et transitoirement l’organisation du génome. Ce modèle pourrait s’appliquer à d’autres types de cellules, comme celles des mammifères, et aider à mieux comprendre la manière dont les chromosomes sont organisés au cours du cycle cellulaire et en quoi cette organisation typique observée en phase S influe en retour sur le fonctionnement de la cellule.
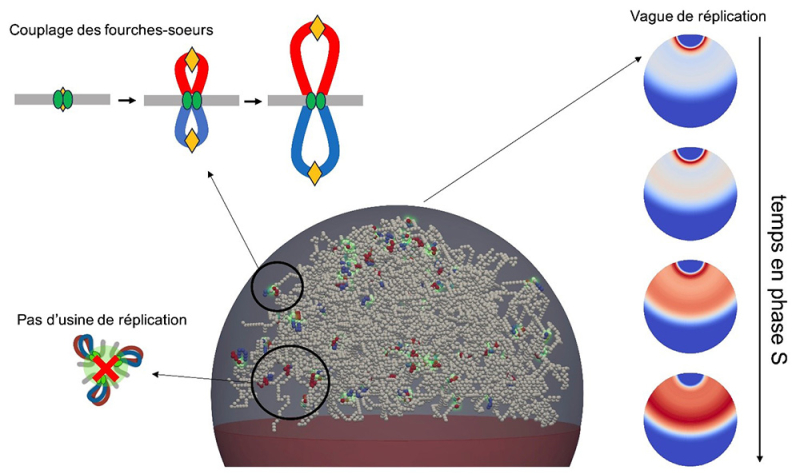
Figure : (Centre, Bas) Représentation de l’organisation des chromosomes en début de phase S chez la levure, issue de simulation numérique. (Gauche, Haut) Schéma illustrant la formation de boucles dynamiques autour des origines de réplication (losange jaune) due à l’interaction entre les fourches-sœurs (ovales verts) réplicant l’ADN. (Gauche, Bas) Les paires de fourches-soeurs ne forment pas d’usine de réplication à plus grande échelle. (Droite) Au cours de la phase S, on observe une « vague » de réplication partant d’un pôle du noyau et qui se « propage » vers le centre du noyau au cours du temps.
En savoir plus : D'Asaro D, Arbona JM, Piveteau V, Piazza A, Vaillant C, Jost D. Genome-wide modeling of DNA replication in space and time confirms the emergence of replication specific patterns in vivo in eukaryotes. Genome Biol. 2025 Dec 22;26(1):431. doi: 10.1186/s13059-025-03872-4. PMID: 41430292.
Contact
Laboratoire
Laboratoire de biologie et modélisation de la cellule (CNRS/ENS de Lyon/INSERM/Univ Lyon 1)
46 Allée d’Italie 69007 Lyon
