Une répartition inégale des mitochondries initie la neurogenèse
Dans un article publié dans Nature Communications, des scientifiques montrent que les mitochondries, organites bien connus pour leur rôle dans le métabolisme cellulaire, ne sont pas distribuées au hasard lors des divisions des cellules souches neurales, à l’origine des cellules du système nerveux. En utilisant l’embryon de poulet comme modèle, ils démontrent que leur répartition inégale est nécessaire et suffisante pour initier la différenciation cellulaire, une étape clé du développement du système nerveux.
Divisions asymétriques : un moment clé pour le démarrage de la neurogenèse
Au cours du développement embryonnaire, l'étonnante diversité des types cellulaires qui composent le système nerveux émerge d'un réservoir limité de cellules souches neurales également appelés progéniteurs neuraux. Dans un premier temps, ces cellules se multiplient de manière exponentielle afin d’amplifier le réservoir de progéniteurs. Puis, au début de la neurogenèse, leur mode de division évolue progressivement vers des divisions asymétriques, capables de produire à la fois une cellule différenciée et une cellule qui conserve un état progéniteur. Ce type de division repose sur la ségrégation inégale de déterminants d’identité cellulaire entre les deux cellules filles. Leur nature reste encore peu connue chez les vertébrés malgré une recherche active dans ce domaine.
La répartition des mitochondries oriente-t-elle le devenir de la descendance des progéniteurs neuraux ?
Ces dernières années, les mitochondries, organites cellulaires essentiels au métabolisme et à la production d’énergie, ont émergé comme des acteurs majeurs des décisions de destin cellulaire dans plusieurs modèles. Lors de la neurogenèse, un profond remodelage de leurs fonctions accompagne la transition entre progéniteur et neurone. Une question demeurait toutefois ouverte : ce rôle des mitochondries intervient-il dès la division des progéniteurs, en influençant différemment le devenir des deux cellules filles ?
Pour y répondre, dans un article publié dans la revue Nature Communications, les scientifiques ont utilisé une technique d’imagerie en temps réel par fluorescence dans la moelle épinière de l’embryon de poulet, technique permettant un suivi dynamique de la répartition des mitochondries lors des divisions cellulaires in vivo.
Une ségrégation mitochondriale liée au destin cellulaire
Leurs observations révèlent que la distribution des mitochondries est d’abord majoritairement égale, puis devient progressivement inégale en parallèle de l’apparition des divisions asymétriques. Manipuler expérimentalement la proportion de divisions asymétriques entraîne d’ailleurs une modification correspondante de la répartition mitochondriale, établissant un lien étroit entre ces deux phénomènes.
Le suivi direct du devenir des cellules sœurs montre que, dans la majorité des divisions asymétriques, l’héritage mitochondrial est inégal : la cellule recevant la plus faible quantité de mitochondries se différencie en neurone, tandis que sa sœur conserve des caractéristiques de progéniteur.
Forcer l’inégalité pour déclencher un destin neuronal
Pour aller au-delà de la corrélation, les scientifiques ont utilisé un système chémogénétique afin de manipuler spécifiquement le transport mitochondrial durant la division cellulaire. En imposant une distribution inégale à un stade où les divisions symétriques prédominent, ils montrent que cette seule inégalité est suffisante pour induire de façon prématurée un destin neuronal dans l'une des cellules filles.
Ces résultats démontrent ainsi de façon directe, avec une résolution cellulaire, le rôle causal d'un héritage mitochondrial différentiel dans la différenciation neuronale in vivo chez les vertébrés.
Fait notable, ce n’est pas le volume absolu de mitochondries hérité par une cellule qui semble décisif, mais le volume relatif par rapport à sa cellule sœur. Les scientifiques suggèrent que cette différence pourrait influencer le dialogue entre cellules sœurs, participant ainsi à l’acquisition de destins identiques ou divergents.
Un nouveau déterminant d’identité cellulaire
En identifiant la ségrégation inégale des mitochondries comme un déterminant d’identité cellulaire, cette étude apporte une nouvelle clé de compréhension des fonctions des mitochondries dans le neurodéveloppement. Plus largement, elle suggère que ce mécanisme pourrait représenter un régulateur général des divisions asymétriques dans d’autres tissus.
Compte tenu de la diversité des fonctions mitochondriales (métaboliques, énergétiques, transcriptionnelles ou traductionnelles) ce travail ouvre de nouvelles perspectives pour décrypter les événements précoces qui gouvernent l’équilibre entre prolifération et différenciation au cours du développement.
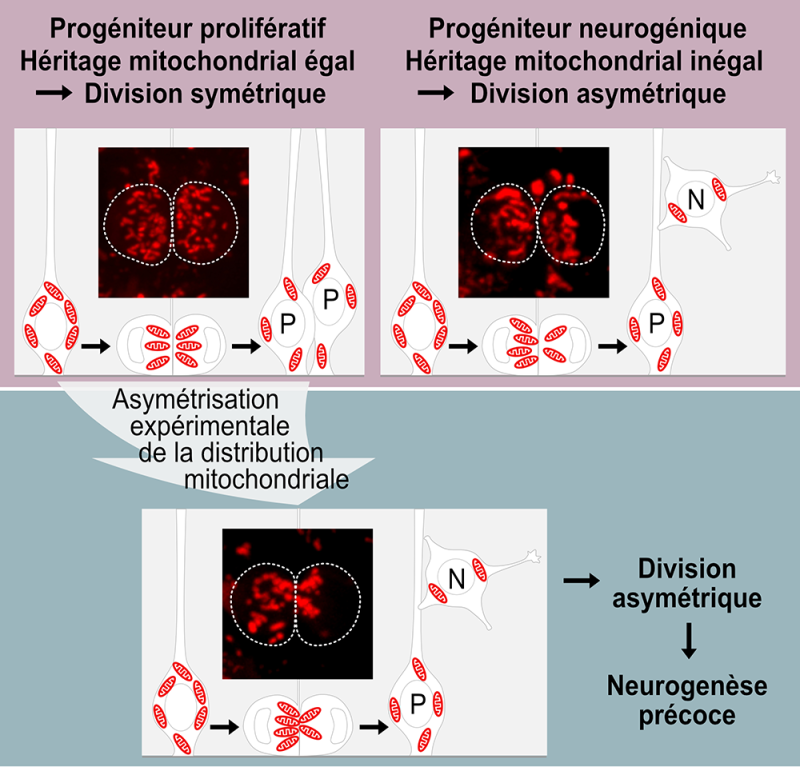
Figure : Lors des stades précoces de développement du tube neural de l'embryon de poulet, les progéniteurs s'amplifient par des divisions symétriques donnant naissance à deux progéniteurs. La ségrégation mitochondriale au cours de la mitose est égale (haut, gauche). Au cours de la neurogenèse, la transition vers un mode de division asymétrique produisant un neurone et un progéniteur est marquée par l'apparition d'une ségrégation inégale des mitochondries, la cellule fille en héritant le moins se différenciant (haut, droite). Forcer cette ségrégation inégale, en modifiant le transport de ces organelles au cours de la mitose, lorsque les divisions symétriques prédominent est suffisant pour induire un destin différentiel des cellules filles et une neurogenèse prématurée (bas). Les encarts montrent les mitochondries (en rouge) héritées par chacune des cellules sœurs dont le contour est marqué par une ligne pointillée.
En savoir plus : Bunel B, Leclercq R, Goïame R, Gautier A, Morin X, Fischer E. Unequal mitochondrial segregation promotes asymmetric fates during neurogenesis. Nat Commun. 2025 Dec 15;16(1):11049. doi: 10.1038/s41467-025-66932-0. PMID: 41398154; PMCID: PMC12706016.
Contact
Laboratoire
Institut de biologie de l’École normale supérieure - IBENS (CNRS/ENS-PSL/Inserm)
46 Rue d'Ulm
75005 Paris